某温度时,在3L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
(1)该反应的化学方程式: ;
(2)反应开始至2min末,X的反应速率为 ;
(3)该反应是由 开始反应的。(正反应逆反应正逆反应同时。)
有机物A(C6H8O4)为食品包装袋内的常用防腐剂。A中以使溴水褪色,A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状态下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)B分子所含官能团的名称是___________________________________________________。
(2)B分子中没有支链,其结构简式是_____________________________________________。
(3)A的结构简式是_____________________________________________________________。
(4)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
B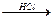 C
C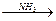 天门冬氨酸
天门冬氨酸
天门冬氨酸的结构简式是________________________________________________________。
(1)由2个C原子、1个O原子、1个N原子和若干个H原子组成的共价化合物,H的原子数目最多为_________个,试写出其中一例的结构简式_______________________。
(2)若某共价化合物分子只含有C、N、H三种元素,且以n(C)和n(N)分别表示C和N的原子数目,则H原子数目最多等于_________。
(3)若某共价化合物分子中只含有C、N、O、H四种元素,且以n(C)、n(N)和n(O)分别表示C、N和O的原子数目,则H原子数目最多等于。
天然蛋白质水解产物中含物质A。A由C、H、O、N元素组成,能与NaOH反应,也能与盐酸反应。在一定条件下,2分子A发生缩合反应生成B和1个水分子,B的式量为312。当蛋白质与浓硝酸反应时显黄色。据此推断:A的结构简式为________;B的结构简式为________。
①
②将A进行下图所示的反应,其中C和C′是同系物,C′是甲酸(HCOOH)
完成下列问题:
(1)C和D′属于________(填入编号,以下同)
①同系物 ②同分异构体 ③同类物质 ④同素异形体
(2)D′和E分别属于哪一类化合物:D′_________,E_________。
①多元醇 ②醛 ③不饱和羧酸 ④多元羧酸 ⑤酯
(3)写出结构简式:A_________,F__________,H___________。
(4)写出反应类型:反应Ⅰ__________,反应Ⅱ____________。
(5)写出下列转化的化学方程式:
A→E:________________________________________________________________
A→B:________________________________________________________________
(1)称取乳酸0.90g,在某种状况下使其完全汽化,已知相同状况下同体积氢气为0.02g。则乳酸的相对分子质量为_________。
(2)若将上述乳酸蒸气在氧气中燃烧只生成CO2和H2O(g),当全部被碱石灰吸收时,碱石灰增重1.86g,若将此产物通入过量石灰水中,则会产生3.00g白色沉淀。则乳酸的分子式为_________。
(3)乳酸分子能发生自身酯化反应,其催化氧化产物不能发生银镜反应,葡萄糖发酵只生成乳酸,试写出生成乳酸的化学方程式______________________________________________
_______________________________________________________________________________。
(4)写出乳酸在催化剂作用下发生反应,生成化学式为C6H8O4的环状酯的结构简式______。