目前,我省多地正在积极推广使用太阳能。常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Cu+在基态时的价电子排布式为______。
(2)砷、碲是第四周期的相邻元素,已知砷的第一电离能(947kj • mol-1)大于碲(941 kj • mol-1)。请从原子结构的角度加以解释_________。
(3)As2O3俗名砒霜,是一种剧毒物质。法医检验砒霜中毒的方法是:向试样中加入锌粉和盐酸,如果有砒霜,将生成无色气体AsH3,将气体导入热玻璃管会分解成亮黑色的“砷镜”,这就是著名的“马氏验砷法”。请用化学方程式表示检验原理:
__________________、__________________
(4)硼酸(H3BO3)在水溶液中易结合一个OH—生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为____________。
②[B(OH)4]-的结构式为____________。
(5)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。
①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是______ (用化学式表示
②立方氮化硼晶体的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361. 5 pm。
立方氮化硼晶胞中含有______个氮原子、______个硼原子,立方氮化硼的密度是______g • cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(9分)Ⅰ:选择一种试剂鉴别下列各组物质,将所选试剂的化学式或名称写在横线上:
①苯、甲苯▲②苯、硝基苯、乙醇▲
③苯酚溶液、己烯、己烷、醋酸溶液▲
Ⅱ:为了探究苯酚和乙醇分子中羟基上氢原子的活泼性,甲、乙两位同学分别设计如下甲、乙两方案。
方案甲:
实验1:取少量无水乙醚于试管中,加入少量金属钠。
实验2:各取3mL无水乙醚于试管中,分别加入少量等物质的量的苯酚和乙醇,再投入大小相同的钠块。
方案乙:
各取少量等物质的苯酚和乙醇于试管中,均在60℃的水浴加热,待苯酚熔化后,各放入相同大小的一小块金属钠。(已知:苯酚的密度为1.07g/mL)
(1)方案甲设计实验1的目的是▲。
(2)方案乙中观察到:在乙醇中,钠很快与乙醇反应产生气体,溶液保持澄清;在苯酚中,钠块表面有少量气泡,且表面产生白色悬浮物,最后白色悬浮物充满苯酚熔融液。
①实验中观察到的白色悬浮物为▲;
②苯酚熔融液与钠的反应速率不如无水乙醇与钠的反应快,其可能原因有
______▲______、_______▲______。
(9分)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。
(1)A的结构简式为▲;
(2)A中的碳原子是否都处于同一平面?▲(填 “是”或者“不是”);
“是”或者“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。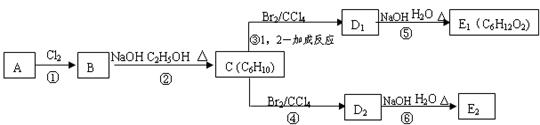
反应②的化学方程式为▲;C的化学名称为▲;
E2的结构简式是▲;④、⑥的反应类型依次是▲
 。
。
(7分)A、B、C、D四种烃分子中均含有8个氢原子,其中A、B常温下呈气态, C 、D呈液态。
(1)A是符合上述条件中相对分子质量最小的,则A的分子式为▲;
(2)B属于链状单烯烃,且与HBr加成的产物只有一种,试写出B与HBr反应的化学方程式▲。
(3)C属于芳香烃,1mol C最多能和3molH2加成,试写出C的结构简式▲。
(4)已知: ;
;
烃D存在如下转化关系: (唯一产物)
(唯一产物)
试写出D的结构简式▲。
(8分)有人设想合成具有以下结构的烃分子.
(1)结构D显然是不可能合成的,原因是 ▲.
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构,金刚烷的分子式为 ▲
(3)B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是 ▲
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)C的一种属于芳香烃的同分异构体是生产某塑 料的单体,写出合成该塑料的化学方式 ▲
料的单体,写出合成该塑料的化学方式 ▲
(9分)根据要求填空:
(1)写出下列有机物的键线式: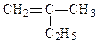 _____▲ ______CH3CH2CH2COOH __▲ _______
_____▲ ______CH3CH2CH2COOH __▲ _______
(2)写出有机物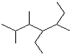 的名称 ▲
的名称 ▲
(3)写出下列原子团的电子式:①甲基 ▲②氢氧根离子 ▲
(4)在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”。C7H16的同分异构体中具有“手性碳原子”的有___▲ ____种.
(5)某有机高分子化合物的结构片段如下: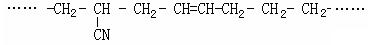
则合成它的单体是▲、▲、▲