某化学反应的能量变化如图所示。下列有关叙述正确的是( )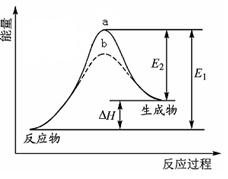
| A.该反应的反应热△H=E2-E1 |
| B.a、b分别对应有催化剂和无催化剂的能量变化 |
| C.催化剂能降低反应的活化能 |
| D.催化剂能改变反应的焓变 |
反应2X(g)+Y(g) 2Z(g)+Q,在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n与反应时间t的关系如下图所示。下列判断正确的是( )
2Z(g)+Q,在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n与反应时间t的关系如下图所示。下列判断正确的是( )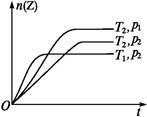
| A.T1<T2,p1<p2 | B.T1<T2,p1>p2 |
| C.T1>T2,p1>p2 | D.T1>T2,p1<p2 |
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g) 2c(g) ΔH1<0
2c(g) ΔH1<0
x(g)+3y(g) 2z(g) ΔH2>0
2z(g) ΔH2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( )
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
已知反应:A(g)+3B(g) 2C(g)是放热反应,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是( )
2C(g)是放热反应,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是( )
| A.正反应速率增大,逆反应速率变小,平衡向正反应方向移动 |
| B.正反应速率变小,逆反应速率增大,平衡向逆反应方向移动 |
| C.正反应速率和逆反应速率都变小,平衡向正反应方向移动 |
| D.正反应速率和逆反应速率都变小,平衡向逆反应方向移动 |
对处于平衡状态的反应:2A(g)+B(g) 2C(g)(已知反应为放热反应),下列叙述正确的是( )
2C(g)(已知反应为放热反应),下列叙述正确的是( )
| A.增大压强,v(正)增大,v(逆)减小 |
| B.升高温度,v(正)减小,v(逆)增大 |
| C.增大A浓度的瞬间,v(正)增大,v(逆)不变 |
| D.增大A浓度的瞬间,v(正)增大而v(逆)减小 |
下图是关于反应A2(g)+3B2(g) 2C(g)(正反应为放热反应)的平衡移动图像,影响平衡移动的原因可能是( )
2C(g)(正反应为放热反应)的平衡移动图像,影响平衡移动的原因可能是( )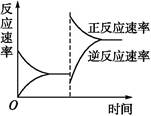
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |