工业上以软锰矿为原料,利用烧结烟气中的SO2制备MnSO4·H2O的流程如下: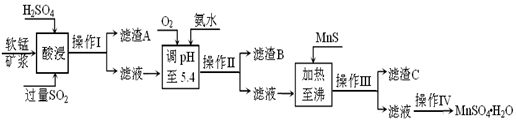
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。酸浸过程发生反应:MemOn+H+→Me(2n/m)++H2O,Me表示Fe、 Al、 Zn、 Cu等。25℃时部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
CuS |
ZnS |
MnS |
FeS |
| pH |
5.2 |
3.2 |
9.7 |
10.4 |
6.7 |
8.0 |
≥-0.42 |
≥2.5 |
≥7 |
≥7 |
回答下列问题:
(1)酸浸时SO2将MnO2还原为MnSO4,其离子方程式为 。
酸浸时SO2的吸收率与pH和温度的关系如下图,为提高SO2的吸收率,酸浸适宜的条件是 。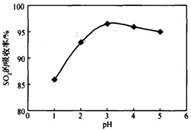
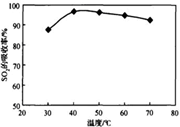
图1: SO2的吸收率与 pH值的关系 图2: SO2的吸收率与温度的关系
(2)滤渣B的主要成分是 。
(3)加入MnS的目的是 。
(4)操作IV的步骤为 、 、过滤、洗涤、干燥。
(5)MnO2的生产方法之一是以石墨为电极,在不断搅拌情况下,电解酸化的MnSO4溶液,阳极的电极反应式为: 。
(6)已知金属离子浓度小于1.0×10-5mol/L时认为已经完全沉淀,根据表格数据,计算25℃时Zn(OH)2溶度积Ksp为 (不需计算过程,计算结果保留两位有效数字)。
(15分)X、Y、Z、W是四种短周期元素,X原子的M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;2的最外层电子数与核外电子总数之比为5:7;W元素最高正价为+7价。
(1)元素W在周期表中的位置是_______________
(2)X、W两种元素的气态氢化物中,稳定性强的是_________(填化学式)
(3)在X2W2分子中,每个原子最外层均达到8电子稳定结构,则X2W2的电子式
为_______________.
(4)由Y2H6、O2、KOH溶液组成的燃料电池中。负极上发生的电极反应为___________________________.
(5)在碱性条件下,用W2将废水中的YZ-转化成Z2和YO32-等,从而使废水得到净化,则
其反应的离子方程式为__________________________________
(6)在常温下,0.2mol YX2(液态)在O2中完全燃烧,生成两种气态氧化物时放出的热量为215kJ,该反应的热化学方程式为_______________________________________.
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1="15" s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用 催化剂 b增大压强 c增大反应物浓度
催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________
(14分)氮是地球上极为丰富的元素,氮元素可形成多种离子,如:N3—、N3—、NH2—、NH4+、N2H5+、N2H62+等。
(1)请画出氮的原子结构示意图___________。
(2)氮的常见氢化物的结构式为________,其空间构型为_______,它极易溶于水的主要原因是_________________,溶于水后显碱性的原因是_______________(用离子方程式说明)
(3)X+中所有电子正好充满K、L两个电子层,它与N3—形成的晶体结构如图26题 l所示。与同一个N3—相连的X+有________个,X的元素符号是________。
(4)最近科学家研制出某元素Z与N元素形成的晶体ZN,已知ZN晶体具有与NaCI相似的晶体结构。图26题-2是从ZN晶体结构图中分割出来的部分结构图,试判断符合ZN晶体结构图的是_______________。
有分别含有A、B、C、D、E、F的六瓶无色溶液,这六种溶质均是中学化学中常用的无机试剂。已知纯E为无色油状液体,溶于水时会放出大量热;B、C、D和F是常见金属的盐,且它们的阴离子均不同。现进行如下实验:
①A的溶液有刺激 性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A的溶液分别加入其它五种物质的溶液中,只有溶有D、F的溶液中有白色沉淀产生;继续加入过量A溶液时,D中沉淀无变化,F中沉淀完全溶解;
③将B的溶液分别加入C、D、E、F的溶液中,含C、D、F的三种溶液中均产生沉淀,E溶液中有无色、无味气体逸出;
④将C的溶液分别加入D、E、F中,均有白色沉淀生成,再加入稀HNO3,沉淀均不溶。根据上述实验信息,请回答下列问题:
(1)确定化学式AC. E
(2)写出F中沉淀完全溶解的化学方程式。
(3)B在溶液中电离出的阴离子为(填化学式),能否确定B在溶液中电离生产的阳离子?若能,写出离子符号,若不能说明进一步鉴定的方法。。
(4)D在溶液中电离出的阴离子为(填化学式),能否确定D在溶液中电离生产的阳离子?若能,写出离子符号,若不能说明进一步鉴定的方法。。
现有甲、乙、丙、丁四种物质,乙、丁的焰色反应均为黄色。丙是一种强酸的酸式盐,将丙加入BaCl2溶液有不溶于盐酸的白色沉淀生成,丁晶体在干燥空气中容易逐渐失去结晶水变成白色粉末。对甲、乙、丙、丁进行下列实验,实验过程和记录如下图所示(无关物质已略去),请回答:
(1)将D溶液蒸干得到的固体是: (写化学式)。
(2)C的结构式是 ,B的电子式为 。
(3)写出D溶液与过量的C反应的离子方程式 。
(4)电解戊的水溶液一段时间后,收集到的三种气体,其一为无色气体 B,另两种是单质,写出电解戊溶液的总方程式: 。
B,另两种是单质,写出电解戊溶液的总方程式: 。
(5)有人设想在适当大小的管道中填充一定量的丁的晶体(摩尔质量在280~300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理: 。