在某锂离子电池中,有一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如右: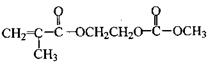
用相对分子质量为56的单烯烃A合成M的方法可设计如下: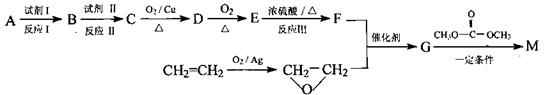
请回答下列问题:
(1)A的结构简式是_______试剂II是________,反应III的化学反应类型是_______。
(2)G在一定条件下反应生成的高聚物是制备隐形眼镜的材料,请写出生成该高聚物的化学反应方程式______________
(3)M与足量氯氧化钠溶液反应的化学方程式是______________
(4)在用E制备F的过程中,2分子的E反应会生成一种副产物,其核磁共振氢谱只有一种吸收峰,该副产物的结构简式为______________。
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为
(2)反应开始至2min、5minZ的平均反应速率为、;
(3)5min后Z的生成速率比5min末Z的生成速率(大、小、相等)。
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示,已知这个反应速率随着溶液中c(H+)增大而加快。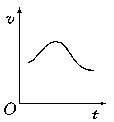
(1)反应开始进行时,反应速率加快的原因是(要求写出化学方程式)
;
(2)反应后期,反应速率下降的原因是
。
(12)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答: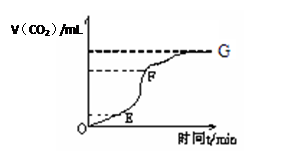
(1)实验过程如下图所示,分析判断:________段化学反应速率最快,_______段收集的二氧化碳气体最多。
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是()
| A.蒸馏水 | B.氯化钠固体 |
| C.氯化钠溶液 | D.浓盐酸 |
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)。
在铝与稀硫酸的反应中,已知10s末,硫酸的浓度减少了0.6mol·L-1,若不考虑反应过程中溶液体积的变化,则10s内生成硫酸铝的平均反应速率是________________________。
已知氯水中有如下平衡: 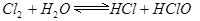 。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象_____________________。可将此针筒
。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象_____________________。可将此针筒
长时间放置,又可能看到何种变化_______;试用平衡观点加以解释。