A-G均为有机化合物,其中A为二卤代烃,相对分子质量为216,碳的质量分数为22.2%。相关转化关系如下: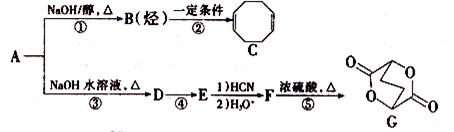
已知:
请回答:
(1)C的核磁共振氢谱有_______个吸收峰。
(2)①、④的反应类型分别为________、______。
(3)下列关于F的说法正确的是_______ (填选项字母)。
a.1 mol F与足量金属钠反应最多生成2 mol H2
b.1 mol F完全燃烧消耗8.5 mol O2
c.能与新制Cu(OH)2反应生成砖红色沉淀
d.能与NaHCO3反应生成CO2
(4)写出下列反应的化学方程式
反应③___________________________________;
反应⑤___________________________________
(5)符合下列条件的同分异构体有_______种,任写其中一种的结构简式_______。
i.与E互为同系物 ii.相对分子质量比E大28
现有常温下的五份溶液:
①0.01 mol·L-1 CH3COOH溶液; ②0.01 mol·L-1 HCl溶液;
③pH=12的氨水; ④pH=12的NaOH溶液;
⑤0.01 mol·L-1 HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是______(填序号,下同),水的电离程度相同的是______;
(2)若将②、③混合后所得溶液pH=7,则消耗溶液的体积:②________③(填“>”、“<”或“=”);
(3)将前四份溶液同等稀释10倍后,溶液的pH:
①________②,③________④ (填“>”、“<”或“=”);
请回答下列问题:
(1)CH4和H2O在催化剂表面发生反应CH4+H2O(g) CO+3H2,该反应在不同温度下的化学平衡常数如下表:
CO+3H2,该反应在不同温度下的化学平衡常数如下表:
| 温度/℃ |
800 |
1 000 |
1 200 |
1 400 |
| 平衡常数 |
0.45 |
1.92 |
276.5 |
1 771.5 |
①该反应是________(填“吸热”或“放热”)反应
②T ℃时,向1 L密闭容器中投入1 mol CH4和1 mol H2O(g),5小时后测得反应体系达到平衡状态,此时c(CH4)=0.5 mol·L-1,计算该温度下CH4+H2O(g) CO+3H2的平衡常数K=______,该温度下达到平衡时H2的平均生成速率为_______________
CO+3H2的平衡常数K=______,该温度下达到平衡时H2的平均生成速率为_______________
(2)常温下,取pH=2的盐酸和醋酸各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸pH变化曲线的是________(填“A”或“B”)。设盐酸中加入的Zn粒质量为m1,醋酸中加入的Zn粒质量为m2。则m1________m2(填“<”、“=”或“>”)。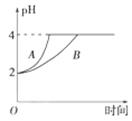
海水中含有非常丰富的化学资,从海水中可提取多种化工原料。下图是某工厂对海水资综合利用的示意图。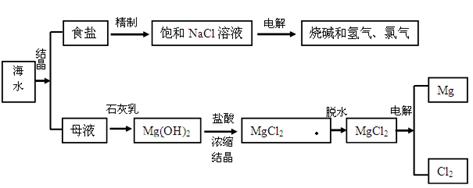
试回答下列问题:
(1)我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为价。
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是①③(填序号)。
(3)写出电解饱和食盐水的化学方程式,当转移0.2mol电子时,阴阳两极生成的气体体积之和是(标准状况下)。
(4)以海边贝壳为原料可以制取石灰乳,贝壳的主要化学成分为(写化学式)。
(5)目前,世界上生产的镁有60%自海水,由“母液”制“镁”的过程中,发生了个复分解反应(填数目)。
(6)电解氯化镁所得的氯气,除用于生产盐酸外,还可以用于制取漂白粉,漂白粉的有效成份
是(写化学式)。
(7)溴主要以Br-形式存在于海水中,提取食盐后剩下的母液(也叫卤水)中,Br-的浓度较大,工业上 制备的Br2的操作步骤为:一定条件下,将Cl2通入卤水中,生成Br2,利用热空气将Br2吹出,Br2可用热空气吹出,其原因是 。
铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
(1)铝在反应中容易失去电子,发生反应(填氧化或还原),生成铝离子,铝离子的结构示意图是。
(2)生产中曾用铝热反应焊接钢轨,写出铝与氧化铁发生反应的化学方程式为并标出电子转移的方向和数目:。
(3)胃舒平是治疗胃酸过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示):;
(4)在同温同压下,等质量的铝分别投入足量的稀盐酸和NaOH溶液中,产生气体的体积之比为。
(5)铝合金在空气中很稳定,可以制造多种建筑型材。向一只小烧杯里加入少量CuSO4溶液,把一小块铝合金浸入溶液中,1~2分钟后将铝合金取出,无明显现象。将另一小块铝合金先放入NaOH溶液里,片刻后取出,用蒸馏水冲洗后浸入CuSO4溶液里,1~2分钟后将铝片取出,发现铝片表面有亮红色的固体附着,NaOH溶液的作用是。
碳及其化合物应用广泛。
I 工业上利用CO和水蒸汽反应制氢气,存在以下平衡:
CO(g)+H2O(g)  CO2(g)+H2(g)△H>0
CO2(g)+H2(g)△H>0
(1)向1L恒容密闭容器中注入CO(g)和H2O(g),830℃时测得部分数据如下表。则该温度下反应的平衡常数K=______________。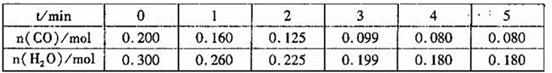
(2)相同条件下,向1L恒容密闭容器中,同时注入2mol CO、2mol H2O(g),1molCO2和1mo1H2,此时v(正 ) __________v(逆)(填“>”“=”或“<”)
(3)上述反应达到平衡时,要提高CO的转化率,可采取的措施是_______(填字母代号)。
| A.升高温度 |
| B.加入催化剂 |
| C.增大压强 |
| D.增加CO的浓度 |
E.及时分离出CO2
II 已知CO(g)+1/2 O2(g)=CO2(g)△H=一141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g)△H=一484 kJ·mol-1
CH3OH(1)+3/2O2(g)=CO2(g)+2H2O(g)△H=一726 kJ·mol-1
(4)用CO(g)、H2(g)化合制得液态甲醇的热化学方程式为___________________________。
III某同学设计了一个甲醇燃料电池,并用该电池电解100mL一定浓度NaCl与CuSO4混合溶液,其装置如图: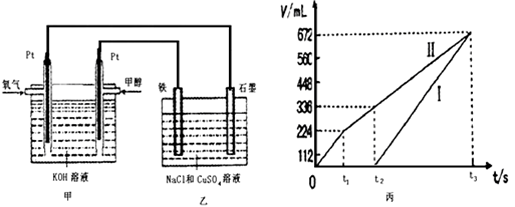
(5)写出甲中通入甲醇这一极的电极反应式__________________________________ 。
(6)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式____________,原混合溶液中CuSO4的物质的量浓度____________mol/L。(假设溶液体积不变)
(7)将在t2时所得的溶液稀释至200mL,该溶液的pH约为___________。