用纯净的碳酸钙跟稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如右图所示,分析判断: 段化学反应速率最快, 段收集的二氧化碳最多。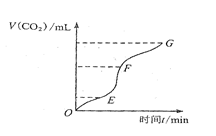
(2)为了减缓上述化学反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
| A.蒸馏水 | B.NaCl固体 | C.NaCl溶液 | D.浓盐酸 |
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?
已知25℃、101 kPa下,稀的强酸与强碱溶液反应的中和热为57.3 kJ/mol。
(1)写出表示稀硫酸与稀烧碱溶液发生反应的中和热的热化学方程式:。
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图。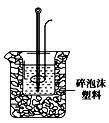
①实验时所需的玻璃仪器除烧杯、量筒外还需:。
②该装置中有一处错误是:,如果用该错误装置测定,结果会(填“偏高”“偏低”“无影响”)
③如果该生用50 mL 0.25 mol/L的稀硫酸与50 mL 0.55 mol/L的稀烧碱溶液,他用试剂的用量的理由是:。在该实验中需要测定某种数据,完成一次实验,需要测定该数据的次数为次。使用正确的装置进行实验,取上述溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃。已知中和后生成的溶液的比热容为4.18J/(g·℃),溶液的密度均为1g/cm3。通过计算可得中和热△H=
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)煤的气化的主要化学反应方程式为:。
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)  CH3OH(g) ΔH=-90.8kJ·mol-1
CH3OH(g) ΔH=-90.8kJ·mol-1
②2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1
③CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=-41.3kJ·mol-1
CO2(g)+H2(g) ΔH=-41.3kJ·mol-1
写出水煤气直接合成二甲醚同时生成CO2的热化学反应方程式。
(3)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是。
a高温高压 b低温低压 c减少CO2的浓度
d增加CO的浓度e分离出二甲醚f加入催化剂
(4)已知反应②2CH3OH(g)  CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
比较此时正、逆反应速率的大小:v(正)v(逆)(填“>”、“<”或“=”),若上述情况达到平衡,此时c(CH3OH)=。
(8分)某温度下,纯水的c(H+)=2×10-7 mol·L-1,则此时c(OH-)为;若温度不变,滴入稀盐酸使c(H+)=5×10-4 mol·L-1则溶液中c(OH-)为,由水电离产生的c(H+)为,此时温度_____(填“高于”、“低于”或“等于”)25℃。
在反应Cu + 4HNO3(浓)="==" Cu(NO3)2 + 2NO2↑ + 2H2O中:
(1)上述反应的离子方程式为。
(2)该反应中氧化剂为_________________,氧化产物为_________________(填化学式)
(3)当该反应有32gCu被消耗,被还原的HNO3的物质的量是_____________,转移的电子的物质的量是_____________。
(10分)现有5瓶透明溶液A、B、C、D、E ,成分均是HCl、BaCl2、NaHSO4、Na2CO3、AgNO3中的一种。已知:
①A与B反应有气体生成②B与C反应有沉淀生成
③C与D反应有沉淀生成④D与E反应有沉淀生成
⑤A与E反应有气体生成⑥ 在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式,下同)是。
(2)A是, C是,E是。
(3)A与E反应的离子方程式是。