用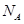 表示阿伏加德罗常数,下列结论能够成立的是
表示阿伏加德罗常数,下列结论能够成立的是
A.2L0.1mol·L-1的NaCO3。溶液中含有CO2- 3的个数是0.2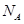 |
B.1 molFe与足量稀硝酸完全反应转移的电子数为2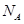 。 。 |
| C.0.2mol·L-1 CuSO4溶液加水稀释至体积增加l倍,其浓度变为0.1mol·L-1 |
| D.常温下pH=5的H2SO3。水溶液中,c(H+): c(SO2- 3)=2:1 |
①pH=0的盐酸 ②0.5 mol·L-1的盐酸③0.1 mol·L-1的NH4Cl溶液 ④0.1 mol·L-1的NaOH溶液 ⑤0.5 mol·L-1的NH4Cl溶液,以上溶液中水电离出的c(H+)由大到小的顺序是
| A.⑤③④②① | B.①②③⑤④ | C.①②③④⑤ | D.⑤③④①② |
室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
| A.该溶液的pH=4 |
| B.升高温度,溶液的pH增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,不正确的是
| A.水电离的c(H+):①=②=③=④ |
| B.若将②、③溶液混合后,pH=7,则消耗溶液的体积:②=③ |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:①最大 |
| D.向溶液中加入100mL水后,溶液的pH:③>④>②>① |
25℃时,水的电离达到平衡:H2O H+ + OH-,下列叙述正确的是
H+ + OH-,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
在25℃时,某稀溶液中由水电离产生的c(OH-)水=10-11mol/L。下列有关该溶液的叙述正确的是
| A.该溶液一定呈酸性 |
| B.该溶液中的c(H+)肯定等于10-3mol/L |
| C.该溶液的pH可能为3,可能为11 |
| D.该溶液一定呈碱性 |