1mol某烃最多能和2molHCl发生加成反应,生成1mol氯代烷,1mol此氯代烷能和8molCl2发生取代反应,生成只含碳元素和氯元素的氯代烷,该烃可能是
| A.CH3CH=CH2 | B.CH2=CHCH=CH2 |
| C.CH3=CHCH3 | D.CH3-C≡CH2-CH3 |
“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。若以铜为原料制取硫酸铜或硝酸铜,下列设计你认为符合“绿色化学”思想的反应路线(用化学方程式表示)是
| A.制CuSO4:Cu + 2H2SO4(浓) = CuSO4 + SO2↑+ 2H2O |
| B.制CuSO4:2Cu + O2= 2CuO; CuO + H2SO4(稀) = CuSO4 + H2O |
| C.制Cu(NO3)2:Cu + 4HNO3(浓)=Cu(NO3)2 +2NO2↑+ 2H2O |
| D.制Cu(NO3)2:3Cu + 8HNO3(稀)=3Cu(NO3)2 +2NO↑+ 4H2O |
下列化学用语的书写正确的是
| A.乙酸的分子式:C2H4O2 |
| B.乙醇的结构简式:C2H6O |
C.F原子结构示意图: |
D.四氯化碳的电子式: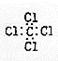 |
下列叙述正确的是
| A.1.00mol NaCl中含有6.02×1023个NaCl分子 |
| B.1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |
| C.欲配制1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠 |
下列有关描述不正确的是
| A.丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B.过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C.常温下,可以用铁或铝制容器盛装浓硫酸和浓硝酸 |
| D.检验某溶液中是否含有SO42-的方法是向该溶液中加入BaCl2溶液,再加入稀HNO3 |
检验SO2气体中是否含有CO2气体应用的方法是
| A.通过石灰水 | B.先通过酸性KMnO4溶液再通过石灰水 |
| C.通过品红溶液 | D.先通过小苏打溶液再通过石灰水 |