硫酸铜常用作农业杀虫剂,如图是利用含铁废铜料生产硫酸铜的工艺,回答下列问题.
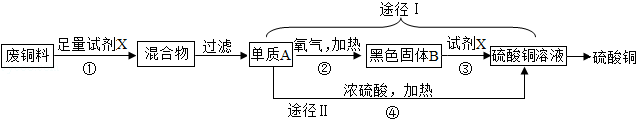
(1)试剂
的化学式是。
(2)途径Ⅰ中,
↑从环保和经济的角度分析,利用途径。(填"Ⅰ"或"Ⅱ")制取硫酸铜更合理;
(3)通常情况下不反应的两种物质,在改变温度和后,也可能发生反应,如果用足量的铜与20.0溶质质量分数为98.0%的浓硫酸在加热条件下充分反应,实际生成二氧化硫的质量是(选填字母)。
| A. |
小于 |
B. |
等于 |
C. |
大于 |
在实验室用电解水的实验来测定水的组成,负极产生的气体体积是正极产生气体体积的2倍,化学反应的文字表达式为,由此可得出的结论是。过氧化氢溶液在常温下(填“能”或“不能”)产生氧气;只给氯酸钾加热(填“能”或“不能”)产生氧气。
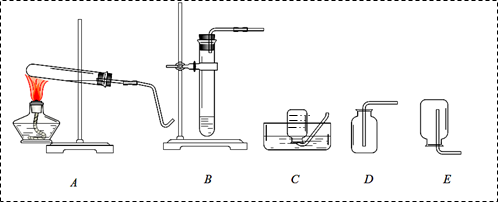
在实验室制备并收集氧气时,如果给一种紫黑色的固体纯净物加热,可选上述装置中
的(填序号,下同),反应的文字表达式为,
如果在该实验中试管破裂了,则可能原因有、.
如果用向上排空气法收集氧气则需要验满,验满的方法是。
下图是研究物质的化学变化时进行的实验,在该实验中可以观察到试管中的现象是,烧杯中的现象是,该发生装置在实验室也可以用来制备氧气,用此装置制备氧气时,化学反应的文字表达式为,化学反应的基本类型为。该发生装置气密性的检查方法是 .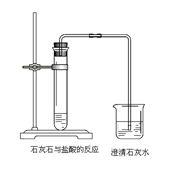
下图是实验室制取气体的常用装置。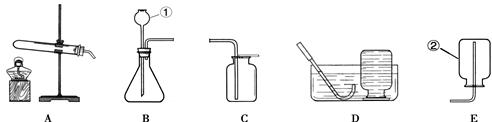
(1)仪器①的名称是。
(2)用高锰酸钾制取氧气的化学方程式为;实验时应在试管口放一团棉花,其作用是;用排水法收集氧气的合适时机是。用右图所示装置收集氧气,氧气应从(填“a”或“b”)端导入。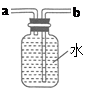
(3)用双氧水制取氧气应选用的发生装置是(填装置字母);发生反应的化学方程式为。
下图是一组用于研究可燃物燃烧条件的对比实验,请回答有关问题:(1)仅由实验1就可得出可燃物燃烧的条件是: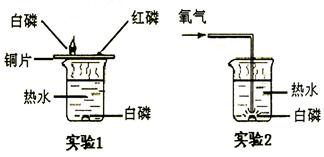
①;②。
(2)通过实验2可以进一步得出燃烧所需要的条件,实验中发生反应的化学方程式为。
(3)一旦室内起火时,如果打开门窗,火反而会烧得更旺,原因是。
扑灭森林火灾的有效方法之一,是将大火蔓延路线前的一片树木砍掉,其灭火原理
是。