实验室制取某些气体所需的装置如图所示,请回答下列问题.
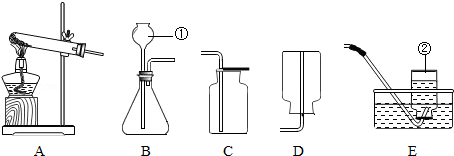
(1)仪器名称:①,②.
(2)选用A装置制取氧气的一个化学方程式为,收集氧气可选用的一种装置是(填字母).
(3)实验室制取二氧化碳气体应选择的发生装置是(填字母),制取二氧化碳的化学方程式为.
在七十五届联合国大会上,中国提出努力争取2060年前实现“碳中和”,实现二氧化碳的“零排放”。化学兴趣小组认为实验室可用氢氧化钠溶液吸收多余的二氧化碳,从而实现实验室二氧化碳的“零排放”。小组同学对吸收后溶液中溶质的成分产生兴趣并进行探究。
【提出问题】氢氧化钠溶液吸收二氧化碳气体后,溶液中溶质的成分是什么?
【查阅资料】
(1)CO2与NaOH溶液反应会生成Na2CO3,当二氧化碳过量时,会继续反应生成NaHCO3。
(2)NaHCO3溶液呈弱碱性,一般不与CaCl2溶液反应,与稀盐酸反应产生气体。
(3)CaCl2溶液呈中性。
【作出猜想】
猜想①NaOH、Na2CO3
猜想②Na2CO3
猜想③Na2CO3、NaHCO3
猜想④NaHCO3
【实验与结论】
|
实验步骤 |
实验现象 |
实验结论 |
|
步骤一:取少量待测液于试管中,加入CaCl2溶液 |
产生白色沉淀 |
猜想 不成立 |
|
步骤二:另取少量待测液于试管中,加入过量CaCl2溶液至不再产生沉淀,过滤,取少量滤液,向其中加入适量稀盐酸 |
气泡产生(填“有”或“无”) |
猜想③不成立 |
|
步骤三:另取步骤二的少量滤液,向其中滴入2~3滴无色酚酞试液 |
试液变红 |
猜想 成立 |
写出步骤一中反应的化学方程式 。
【反思与交流】
反应物的量不同,可能导致生成物的种类不同。
【实验与结论】
|
实验步骤 |
实验现象 |
实验结论 |
|
步骤一:取少量待测液于试管中,加入CaCl2溶液 |
产生白色沉淀,是因为碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,说明溶液中含有碳酸钠 |
猜想④不成立 |
|
步骤二:另取少量待测液于试管中,加入过量CaCl2溶液至不再产生沉淀,过滤,取少量滤液,向其中加入适量稀盐酸 |
稀盐酸能和碳酸氢钠反应生成氯化钠、水和二氧化碳,无气泡产生,说明溶液中不含有碳酸氢钠 |
猜想③不成立 |
|
步骤三:另取步骤二的少量滤液,向其中滴入2~3滴无色酚酞试液 |
试液变红,是因为除去碳酸钠后溶液中仍然含有氢氧化钠,氢氧化钠溶液显碱性,能使酚酞试液变红色,说明溶液中含有氢氧化钠 |
猜想①成立 |
步骤一中碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,反应的化学方程式:
学习小组同学在探究Cu、Al、Ag的活动性顺序时,做了如图两个实验,并由此展开了一系列学习探究活动。
【学习交流】
(1)实验中观察到,甲中铝丝表面附着一层 色固体,乙中溶液颜色变为 色。
(2)你认为通过上述实验 (填“能”或“不能”)得出三种金属的活动性强弱。
【拓展探究】
上述实验后,同学们想进行废液的处理与回收,于是将甲、乙中的溶液倒入同一烧杯中,观察到混合溶液(即废液)澄清透明。同学们认为应该先确定废液中是否含有未反应完的CuSO4和AgNO3,为此,他们进行了实验并记录如下:
|
序号 |
实验操作 |
实验现象 |
实验结论 |
|
实验1 |
取少量废液于试管中,加入 溶液 |
无明显现象 |
废液中没有AgNO3 |
|
实验2 |
取少量废液于试管中,加入Ba(NO3)2溶液 |
产生白色沉淀 |
废液中含有未反应完的CuSO4 |
【反思评价】
讨论后大家一致认为实验2所得结论不合理。你认为理由是 (用化学方程式表示)。
【拓展应用】
同学们尝试从废液中回收铜,将过量铝粉加入废液中,充分反应后过滤,滤液中存在的金属阳离子是 (写离子符号)。

3月16日,沙尘暴席卷我国西北地区,次日多地又遇到降雨。该地某校环境监测实践小组的同学们,对沙尘暴的成因、危害、成分、防护、治理以及雨水酸碱度的异常变化产生了浓厚的兴趣,在老师的指导下,他们紧急立项,开启了项目性学习的探究之旅。
任务一:监测沙尘暴的成因
同学们参与当地环境监测。他们在10米高台上,利用“风向风速器”,测得风速为10m/s时,有大量的沙尘被卷入空中,能见度迅速降低。引发这一自然现象的根本原因是
(写1条)。
任务二:分析沙尘暴的危害
当人暴露于沙尘天气中时,含有各种有毒的化学物质、病菌等的尘土可进入到口、鼻、眼、耳中引发各种疾病。除此之外沙尘暴还会产生的危害是 (写1条)。
任务三:探究沙尘暴的成分
【信息检索】我国西北地区,含有大量钠盐的干涸盐湖和盐碱地总面积约有50万平方公里,为沙尘暴的形成埋下隐患。
【猜想假设】此次沙尘暴中可能含有碳酸钠等碱性物质。
【进行实验】取少量盐碱地的土壤与蒸馏水按1:5的质量比在烧杯中混合,充分搅拌后静置,取上层清液,用如图装置完成如下实验。
|
项耳 |
实验步骤 |
实验现象 |
实验结论 |
|
方案 |
①挤压胶头滴管a,滴入 |
产生白色沉淀 |
沙尘暴中含有Na2CO3,不含NaOH |
|
②挤压胶头滴管b,滴入几滴酚酞溶液 |
酚酞溶液不变色 |
【反思评价】
(1)步骤①中发生反应的化学方程式为 。
(2)自然界的土壤中通常不含NaOH,理由是 。
(3)若加入的X是 (填化学式),则只能证明沙尘暴中含有Na2CO3,而不能确定是否含有NaOH。
任务四:评价雨水pH异常的原因
【数据监测】小组同学在老师的帮助下,从环保部门获得了当地雨水的pH数据。
|
测定时间 |
3月5日 |
3月17日 |
3月28日 |
3月31日 |
|
pH |
5.57 |
5.73 |
5.60 |
5.59 |
【表达交流】3月17日,雨水pH出现异常的原因是 。
【检查进度】该项目性学习还没有进行的探究项目是 。

因发现青蒿素而获诺贝尔奖的科学家屠呦呦还发现了双青蒿素,查阅资料可知,双青蒿素由碳、氢、氧三种元素组成。为测定双青蒿素中碳、氢、氧三种元素的质量比。兴趣小组进行了以下探究。
【设计实验】兴趣小组设计并进行了如图一所示的实验。(装置气密性良好)

将7.1g双青蒿素放在装置C的玻璃管中,燃烧至无固体灰分残留。
(1)装置A、B中盛放的试剂分别是 (填序号)。
①足量NaOH溶液、足量浓硫酸
②足量浓硫酸、足量NaOH溶液
(2)装置F可吸收从装置E的气流中带出来的少量水蒸气,生石灰与水蒸气发生反应的化学方程式是 。
【记录数据】加热前,先通入空气一段时间,再称量装置D的质量、装置E和F的总质量(反应前的质量)。双青蒿素完全反应后,停止加热,继续通入空气一段时间,再次称量装置D的质量、装置E和F的总质量(反应后的质量),实验数据如表所示。
|
装置 |
反应前的质量/g |
反应后的质量/g |
|
D |
74.7 |
80.1 |
|
E和F |
80.3 |
96.8 |
【实验结论】(3)根据表中数据分析,双青蒿素中碳、氢、氧三种元素的质量比是 。
【拓展分析】(4)双青蒿素分子中碳、氢、氧三种原子的个数比是 。
【实验反思】(5)实验过程中,加热前要先通入空气一段时间,该操作的作用是 。
(6)有同学建议,为使实验结果更准确,需要在装置C和D之间增加图二所示的装置,其目的是 。
兴趣小组的同学为探究在空气中久置的某氢氧化钠样品是否变质,设计了如图所示的A、B、C、D四组探究实验。

【查阅资料】氯化钙、氯化钡溶液都呈中性。
【实验探究】取适量该氢氧化钠样品,加足量的水溶解,将得到的溶液分别加入到四支试管中,再向四支试管中分别加入稀盐酸(足量)、酚酞试液、氢氧化钙溶液、氯化钙溶液,如图所示。
【分析与结论】(1)上述四组实验中不能达到实验目的的是 (填字母序号)。
(2)实验A中,观察到 的现象,说明该氢氧化钠样品已经变质。
(3)实验D中,证明该氢氧化钠样品已经变质的反应的化学方程式是 。
【继续探究】实验结束后,同学们将四支试管中反应后的混合物全部倒入一个洁净的大烧杯中(如图),充分搅拌、静置,观察到烧杯内上层清液呈红色,下层有白色沉淀。
【提出问题】上层清液呈红色,说明溶液呈碱性。上层清液中呈碱性的物质是什么?
【猜想与假设】上层清液中呈碱性的物质可能是碳酸钠、氢氧化钙和 三种物质中的一种或两种。
【设计实验】取少量烧杯中的上层清液于试管中,加入过量的氯化钡溶液,观察现象。
【现象与结论】
|
预测现象 |
结论 |
|
①若有白色沉淀生成,溶液呈红色 |
上层清液中呈碱性的物质是
|
|
②若无沉淀生成,溶液呈红色 |
上层清液中呈碱性的物质是氢氧化钙。 |
【实验反思】同学们认为上述预测现象②所得结论不严密,原因是 。