学习小组同学在探究Cu、Al、Ag的活动性顺序时,做了如图两个实验,并由此展开了一系列学习探究活动。
【学习交流】
(1)实验中观察到,甲中铝丝表面附着一层 色固体,乙中溶液颜色变为 色。
(2)你认为通过上述实验 (填“能”或“不能”)得出三种金属的活动性强弱。
【拓展探究】
上述实验后,同学们想进行废液的处理与回收,于是将甲、乙中的溶液倒入同一烧杯中,观察到混合溶液(即废液)澄清透明。同学们认为应该先确定废液中是否含有未反应完的CuSO4和AgNO3,为此,他们进行了实验并记录如下:
序号 |
实验操作 |
实验现象 |
实验结论 |
实验1 |
取少量废液于试管中,加入 溶液 |
无明显现象 |
废液中没有AgNO3 |
实验2 |
取少量废液于试管中,加入Ba(NO3)2溶液 |
产生白色沉淀 |
废液中含有未反应完的CuSO4 |
【反思评价】
讨论后大家一致认为实验2所得结论不合理。你认为理由是 (用化学方程式表示)。
【拓展应用】
同学们尝试从废液中回收铜,将过量铝粉加入废液中,充分反应后过滤,滤液中存在的金属阳离子是 (写离子符号)。

某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”感到非常好奇,设计实验进行探究。
【提出问题】过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
【查阅资料】① 人呼出的气体中主要成分是N2、O2、CO2和水蒸气等。
② CO2 + 2NaOH=Na2CO3 + H2O。
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气。
【进行实验】
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。
(1)实验操作如右图所示。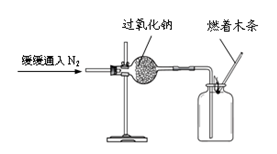
(2)实验现象及结论:观察到________现象,
判断过氧化钠与氮气没有发生反应。
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
(1)同学们在老师的指导下设计了如下图所示装置。其中A装置的作用是_______,发生的变化是________变化。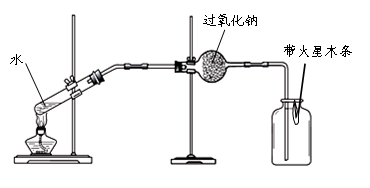
A BC
(2)实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气。
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。
(1)同学们在老师的指导下设计了如下图所示装置。(提示:C装置中的氢氧化钠溶液用于吸收可能未反应的二氧化碳)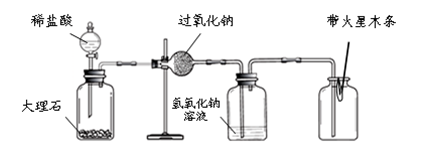
A B C D
(2)实验记录
| 实验操作 |
主要实验现象 |
实验结论及解释 |
|
| ① |
检查装置的气密性。 向装置中加入药品。 |
装置的气密性良好。 |
|
| ② |
打开分液漏斗活塞,向A装置中缓慢加入稀盐酸。 |
A装置中观察到的现象有________,C装置中有气泡出现。 |
A装置中发生反应的化学方程式为________; |
| ③ |
一段时间后用带火星的木条在D内进行检验。 |
带火星的木条复燃。 |
过氧化钠与二氧化碳反应并生成氧气。 |
【实验反思】
(1)根据实验Ⅱ和Ⅲ,过氧化钠与二氧化碳或水蒸气反应后,还产生了另一种物质,该物质是________(填“单质”或“化合物”)。
(2)某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是________。
下图是实验室制取气体常用的实验装置,回答下列有关问题: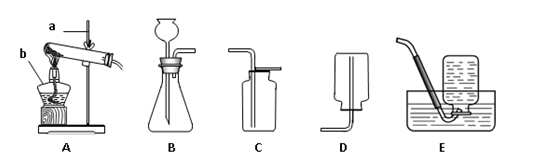
(1)请写出图中标有字母的仪器名称:ab
(2)实验室制取二氧化碳应选用的发生装置是(填字母序号,下同),收集装置是。检验二氧化碳是否已集满的方是。
(3)实验室若用装置B制取氧气,发生反应的化学方程式为。
(4)某活动小组对教材中一氧化碳的化学性质实验并不太满意,于是决定进行创新设计。经查阅资料得知:甲酸(HCOOH)在浓硫酸催化及加热的条件下分解生成一氧化碳气体和水,实验室常用此方法制取一氧化碳。在老师的指导下,同学们设计了一氧化碳的制取、可燃性及还原性的综合实验方案(如下图)。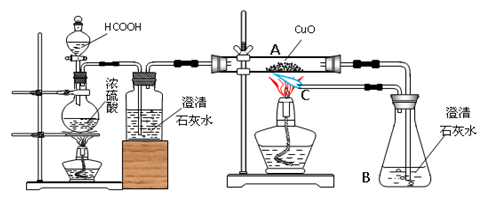
根据题目提供的信息及实验装置图,完成下面相关各项。
①写出实验室制取一氧化碳的化学方程式:。
②写出A、B、C各处的实验现象及反应的化学方程式
| 实验现象 |
化学方程式 |
|
| A |
||
| B |
||
| C |
③说出你对该实验设计的评价(优、缺点),并阐述你的观点:
。
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验。
| 实验编号 |
实验操作 |
实验现象 |
① |
分别在试管A、B中加入 5 mL 5%(溶液浓度) H2O2溶液,各滴入2 滴相同浓度的CuSO4溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 |
试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
| ② |
另取两支试管分别加入5mL 5%H2O2溶液和5 mL 10%H2O2溶液 |
试管A、B中均未明显见到有气泡产生。 |
(1)过氧化氢分解的化学方程式为。
(2)实验①的目的是。
实验中滴加CuSO4溶液的目的是。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你设计的实验方案是。(用实验中所提供的几种试剂)。
(4)对于H2O2分解反应,Fe2(SO4)3溶液也有一定的催化作用。为比较Fe2(SO4)3和CuSO4溶液对H2O2分解的催化效果。某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题: 
如图所示,同学们分别从定性和定量角度进行了比较。
①定性分析:如图甲可通过观察,定性比较得出结论。
②定量分析:用图乙所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是。
(5)通过对上述实验过程的分析,在实验设计时,要考虑_________方法的应用。
实验室中,利用下列装置可以制取某些气体,请回答下列问题。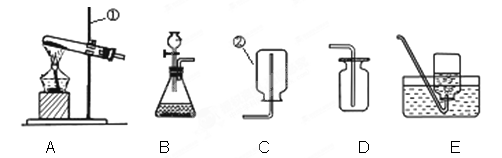
⑴写出带标号的仪器的名称:①;②。
⑵向气体发生装置内加入药品前,应该进行的操作是。
⑶实验室若用高锰酸钾制取氧气,选择的发生装置是;用双氧水制氧气的化学方程式为;
⑷能用C装置收集的气体,必须具备的性质是;
⑸乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取乙炔应选择的发生装置是;收集装置是(此空2分,回答不全将酌情扣分)。
根据下图所示装置回答问题:
(1)用A装置制取氧气,反应的化学方程式为。
(2)实验室若用B装置来制取二氧化碳时,往长颈漏斗中应加入。若用G来收集二氧化碳,二氧化碳应从进(选“a”或“b”)。
(3)制取二氧化碳最好选择的发生装置是(选择“B”或“C”),与另一个装置相比,其优点是:。
(4)硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体。实验室制取H2S气体时,发生装置应选用,收集装置应选用__________ (填仪器编号)。
(5)红旗水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)
有关实验数据如下表:
| 反应前 |
反应后 |
||
| 实验数据 |
烧杯和稀盐酸的质量 |
石灰石样品的质量 |
烧杯和其中混合物的质量 |
| 160 g |
12 g |
167.6 g |
求该石灰石中碳酸钙的质量分数。