氧氮杂 是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质。下面是某研究小组提出的一种氧氮杂
是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质。下面是某研究小组提出的一种氧氮杂 类化合物H的合成路线:
类化合物H的合成路线:

(1)原料A的同分异构体中,含有苯环、且核磁共振氢谱中有4个峰的是 (写出其结构简式)。
(2)反应②的化学方程式是_________________。
(3)③的反应类型是___________。原料D中含有的官能团名称是_________、_________。
(4)原料B俗名“马莱酐”,它是马莱酸(顺丁烯二酸: )的酸酐,
)的酸酐,
它可以经下列变化分别得到苹果酸( )和聚合物Q:
)和聚合物Q:

写出反应I和反应II的化学方程式:___________________、_____________________。
(5)符合下列条件的中间产物F的同分异构体数目是________(不考虑手性异构),写出其中任意一种的结构简式___________。
(i) 能发生银镜反应;
(ii) 分子中含有三取代的苯环结构,其中两个取代基是:—COOCH3和 ,且二者处于对位。
,且二者处于对位。
在一密闭容器中加入A、B进行可逆反应:A(g) + B(g) mC(g), A的转化率(αA)与温度(T)、压强的关系如下图所示:
mC(g), A的转化率(αA)与温度(T)、压强的关系如下图所示:
(1)此反应的正反应是(放热、吸热)反应
(2)若保持其它条件不变,升高温度,C的产率将(变大、变小);
(3)正反应是体积(缩小、增大)的反应,m值为;
(4)若要提高A的转化率,可采取的措施是:(只写两个)。
把在空气中久置的铝片5.0 g投入盛有 500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如下的坐标曲线来表示,回答下列问题:
(1)曲线由0→a段不产生氢气的原因是,有关的化学方程式为;
(2)曲线由a→b段产生氢气的速率较慢的原因是:;
(3)曲线由b→c段,产生氢气的速率增加较快的主要原因:;
(4)曲线由c以后,产生氢气的速率逐渐下降的主要原因:。
(1)下图左表示在密闭容器中反应:2SO2+O2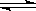 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是;
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是;
b c过程中改变的条件可能是; 若增大压强时,反应速度变化情况画在c~d处. 
(2)发射卫星时可用肼(N2H4)为燃料和二氧化氮做氧化剂,两者反应生成氮气和气态水。
已知:(a) N2 (g) + 2O2 (g) = 2NO2 (g)△H =" +" 67.7kJ/mol
(b) N2H4 (g) +O2 (g) = N2(g) +2H2O (g) △H = -543kJ/mol
(c) 1/2H2 (g) + 1/2F2 (g) = HF (g) △H = -269kJ/mol
(d) H2 (g) + 1/2O2 (g) = H2O (g) △H = -242kJ/mol
①肼和二氧化氮反应的热化学方程式为;
②有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,肼和氟反应的热化学方程式: 。
(14分)汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义。
Ⅰ.①CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g)△H1= —574 kJ·mol- 1.
②CH4(g) + 4NO(g) = 2N2(g)+CO2(g)+2H2O(g)△H2= 一1160 kJ·mol- 1
(1)甲烷直接将NO2还原为N2的热化学方程式为;
Ⅱ.吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):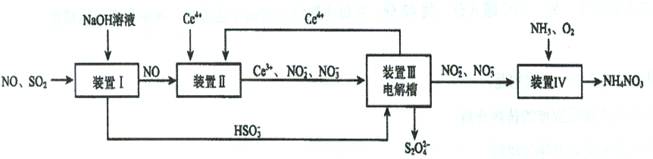
(2)装置Ⅱ中,酸性条件下,NO被Ce 4+ 氧化的产物主要是NO3- 、NO2- ,写出只生成NO3- 的离子方
式;
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
①生成的Ce4+ 从电解槽的(填字母序号)口流出;
②生成S2O42 - 的电极反应式为;
(4)已知进入装置Ⅳ的溶液中,NO2- 的浓度为a g·L- 1 ,要使1m3该溶液中的NO2- 完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的O2L。(用含a代数式表示,计算结果保留整数)
(16分)A、B、C、D、E为原子序数依次增大的短周期元素,其中只有一种是金属元素。A、D元素原子最外层电子数相同,且A和D可形成离子化合物,C2 - 和D+ 具有相同的电子数,E元素的最高正化合价与最低负化合价之和为2。由这些元素组成的物质,其组成和结构信息如下表:
请用化学用语回答下列问题:
(1) D+ 的结构示意图为;
(2) C、D、E的氢化物按熔点由高到低排列的顺序为;
(3) 乙属于分子(填“极性”或“非极性”),丁的电子式为,
(4) 将少量甲投入到AlCl3溶液中反应的离子方程式为;
(5) 丙属于晶体,丙中每个原子均形成4个共价键,其中有一个配位键,提供空轨道的是;
氮化硼晶体的熔点要比丙晶体高,其原因是。