金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g)  W (s) + 3H2O (g) 请回答下列问题:
W (s) + 3H2O (g) 请回答下列问题:
(1)在一定温度下进行上述反应,若反应容器的容积为0.5 L,2min后达到平衡,测得固体的质量减少了4.80 g,则H2的平均反应速率_________;该反应的平衡常数表达式K=___________
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为__________;随温度的升高,H2与水蒸气的体积比减小,则该反应为 ____(填“吸热”或“放热”) 反应。
(3)一定温度下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是________。
A.混合气体的总压强保持不变 B.v正(H20)= v正(H2)
C.混合气体的密度保持不变 D.混合气体的平均式量保持不变
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) 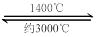 WI4 (g)。下列说法正确的有__________。
WI4 (g)。下列说法正确的有__________。
A.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.灯管内的I2可循环使用
(1)依据氧化还原反应:2Ag+(aq) + Cu(s) ="=" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
①电极X的材料是 ;电解质溶液Y是;
;电解质溶液Y是;
②银电极为电池的极,发生 的电极反应式为;X电极上发生的电极反应式为;
的电极反应式为;X电极上发生的电极反应式为;
③外电路中的电子是从电极流向电极。
(2)物质Z是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应。
①若Z为氧化物,X的化学式是___________________________。
②若Z为单质,Z与NaOH溶液反应的离子方程式为___________________________________。
③若Z与稀硫酸反应生成无色没有气味的气体A,与氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。
Z与稀硫酸反应的离子方程式是______________________________________;
Z与足量氢氧化钠溶液加热的离子方程式是__________________________。
某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
回答下列问 题:
题:
(1)混合物中是否存在FeCl2:____________(填“是”或“否”)。
(2)混合物中是否存在(NH4)2SO4:____________(填“是”或“否”)。
(3)写出反应⑤的离子方程式:________ ________________。
________________。
(4)请根据图中数据分析,原固体混合物的成分为(写化学式)
实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是Na2CO3溶液,为确定甲、乙的成分及其物质的量浓度,现操作如下:
①取25.00 mL甲溶液,向其中缓慢滴加乙溶液15.00mL,其收集到气体224mL。
②另取15.00mL乙溶液,向其中缓慢滴加甲溶液25.00mL,共收集到气体112mL。
上述气体体积均已换算为标准状况,CO2在溶液中的少量溶解忽略不计。请根据实验数据填空:
(1)甲是 ,甲溶液中溶质的物质的量浓度为,乙溶液中溶质的物质的量浓度为。
,甲溶液中溶质的物质的量浓度为,乙溶液中溶质的物质的量浓度为。
(2)将n mL的甲溶液与等体积的乙溶液按各种可能的方式混合,产生的气体体积为
V mL(标准状况),则V的取值范围为。
物质A-L之间的转化关系如图,部分反应物和生成物及反应条件已省略。化合物A是由三种元素组成的一种矿石的主要成分。A在氧气中高温煅烧生成B、C、D。B为砖红色固体,D、I均为红色固体,E、I、K是三种常见金属,其中组成E的元素是地壳中含量最高的金属元素。L可作净水剂,向L溶液中加入BaCl2溶液,会生成不溶于稀硝酸的白色沉淀,H溶液呈蓝色。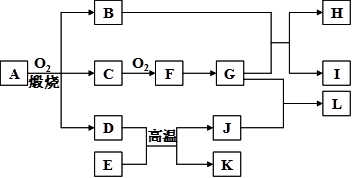
请回答下列问题:
(1)写出E和G的化学式:E、G。
(2)L可用作净水剂的原因是(用离子方程式表示)。
(3)写出B和G反应的化学方程式。
(4)D+E→K+J的反应中放出大量的热,这类反应被称为反应,举出这类反应的一个应用实例:。
(5)A的相对分子质量为184,A与O2反应得到B、C、D三种物质的物质的量之比为1︰4︰1 ,某种检验葡萄糖的反应中含有B生成,则A的化学式为。
,某种检验葡萄糖的反应中含有B生成,则A的化学式为。
(6)过量的I与含n molG的浓G溶液共热生成m molC,若给反应后的溶液中加入足量的K的粉末,则溶解掉K的质量为g(用含n和m的代数式表示)。
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过分析比较,认为无需检验就可判断其中必有的两种物质是
和。(填化学式)
(2)为了确定X,现将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕色沉淀,向该沉淀中滴入稀硝酸,沉淀部分溶解,最后留有白色沉淀不再溶解。则:
①X为。
A.SO32- B.SO42-C.CH3COO- D.SiO32-
②A中的化学键类型为
③将0.02mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为(精确到0.1g)。
④利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀硫酸,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的(填相应的离子符号)。有关反应的离子方程式为