事实上,许多氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2 +SO2 →Na2SO4;2Na2O2 +2SO3→2Na2SO4 +O2 ,据此你认为下列反应方程式中正确的是
| A.2Na2O2 + 2N2O3→4NaNO2 + O2 | B.Na2O2 + 2NO2 →2NaNO2 + O2 |
| C.Na2O2 + N2O4→2NaNO3 | D.2Na2O2 + 2 Mn2O7 → 4NaMnO4 + O2 |
下列现象或事实可用同一原理解释的是
| A.浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| B.SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同 |
| C.水玻璃和Na2SO3长期暴露在空气中变质 |
| D.常温下铁分别加入浓硫酸和浓硝酸中均无明显现象 |
下列说法正确的是
| A.酸雨形成的主要原因是汽车尾气的任意排放 |
| B.填埋法是垃圾处理的最佳方法 |
| C.维生素C受热更易被氧化,故有些新鲜蔬菜生吃较好 |
| D.淀粉、纤维素、蛋白质和油脂均属于天然高分子化合物 |
根据下列实验内得出的结论正确的是
| 选项 |
实验内容 |
结论 |
| A. |
一红棕色气体能使湿润的KI–淀粉试纸变蓝 |
证明该红棕色气体一定为溴蒸气 |
| B. |
向某溶液中加入氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有SO42- |
| C. |
铝箔在酒精灯火焰上加热熔化但不滴落 |
说明铝箔表面氧化铝膜熔点高于铝 |
| D. |
取少量待测晶体于试管中,加浓的NaOH溶液并加热,试管口湿润的红色石蕊试纸变蓝 |
证明晶体成分中含有NH4+ |
下列装置或操作能达到目的的是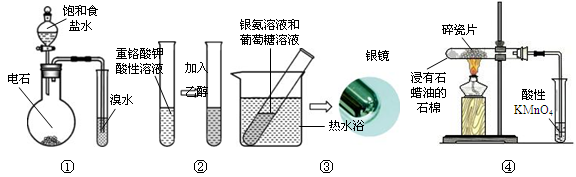
| A.装置①:制取乙炔并验证炔烃的性质 |
| B.装置②:检验乙醇的氧化性,溶液颜色从绿色变成橙色 |
| C.装置③:验证葡萄糖分子中含有醛基官能团 |
| D.装置④:酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
下列离子方程式正确的是
| A.金属钠与水反应:Na+H2O = Na++OH-+H2↑ |
| B.铜粉溶于氯化铁溶液中:Cu + 2Fe3+ = 2Fe2+ + Cu2+ |
| C.氯气与冷氢氧化钠溶液反应:Cl2 + 2OH-= Cl-+ ClO-+ H2O |
| D.向氯化铝溶液中加入过量氨水:4OH-+ Al3+ = AlO2-+2H2O |