常温下,NaOH溶液与未知浓度的醋酸溶液等体积混合后,向溶液中滴加甲基橙试液,溶液变红,下列情况可能出现的是
| A.混合溶液中:4<pH<5 |
| B.混合溶液中离子浓度:c(Na+)+c(H+)≤c(CH3COO-)+c(OH-) |
| C.混合前溶液的pH:pH(CH3COOH)+pH(NaOH)<14 |
| D.混合溶液中粒子浓度:c(Na+)= c(CH3COO-)+c(CH3COOH) |
将等物质的量的X.Y气体充入一容积可变的密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)+2M(s)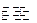 2Z(g);
2Z(g);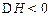 。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是()
。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是()
| 改变的条件 |
正.逆反应速率变化 |
新平衡与原平衡比较 |
|
| A |
升高温度 |
逆反应速率增大量大于正反应速率增大量 |
X的体积分数增大 |
| B |
增大压强 |
正反应速率增大,逆反应速率减小 |
Z的浓度不变 |
| C |
减小压强 |
正.逆反应速率都减小 |
Y的体积分数变大 |
| D |
充入一定量的Z |
逆反应速率增大 |
X的体积分数变大 |
下列选项中,对于指定项目的数目前后相等的是()
| A.电子数:17gOH—与1mol-OH |
B.双键数目:1mol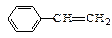 与4mol C2H4 与4mol C2H4 |
| C.分子数:常温常压下16g氧气与4g氦气 |
| D.阴离子总数:72gCaO2与62g Na2O |
制印刷电路时常用氯化铁溶液作腐蚀液,有关反应为2FeCl3+Cu=2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯中不可能出现的是()
| A.有铜粉无铁粉 | B.有铁粉无铜粉 |
| C.铁粉.铜粉都有 | D.铁粉.铜粉都无 |
下列有关说法中正确的是()
| A.我们把微粒大小在1nm~100nm的粒子称为胶体 |
| B.若水溶液中,c(H+)>c(OH—),则溶液一定呈酸性 |
| C.氧化剂在反应中化合价降得越多,则其氧化性就越强 |
| D.若ⅡA族某元素的原子序数为m,则同周期ⅢA族元素的原子序数有可能为m+10 |
将1mol SO2和1mol O2通入容积固定的密闭容器中,在一定条件下反应达到平衡,平衡时SO3物质的量为0.3mol。此时若移走0.5mol SO2和0.5mol O2,则反应达到新平衡时SO3的物质的量是()
| A.0.3mol | B.0.15mol |
| C.小于0.15mol | D.大于0.15mol且小于0.3mol |