增塑剂是一种增加材料的柔软性或使材料液化的添加剂,不能用于食品、酒类等行业。DBP是增塑剂的一种,可由下列路线合成。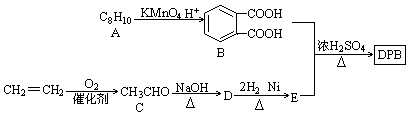
已知以下信息:
①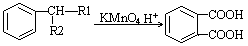
②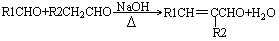
(—R1、一R2表示氢原子或烃基)
(1)A的结构简式 ,D→E的反应类型 。
(2)B的名称是 ,D中含有的官能团名称是 。
(3)由B和E合成DBP的化学方程式 。
(4)写出同时符合下列条件的B的所有同分异构体结构简式
①能和NaHCO3溶液反应生成CO2 ③能使FeC13溶液发生显色反应
②能发生银镜反应 ④苯环上含碳基团处于对位
下图是测定植物某一生命活动过程的装置,A瓶中的氢氧化钠的作用是______________,B瓶中的石灰水的作用是___________,D瓶中出现的现象是_____________。此实验说明植物具有_________性质。
为了检验糖尿病病人的尿液中是否含有葡萄糖,并判断病情轻重,应选用下列试剂中的(填序号),进行的操作是________(填序号),并根据病情的轻重(任选一种),在结论中用不同数目的“+”号表示。
| 试剂 |
操作步骤 |
发生现象 |
结论 |
| ①氢氧化铜 |
A.将尿液与试剂混合振荡 |
甲.蓝色溶液 |
|
| 乙.生成绿色沉淀 |
|||
| ②斐林试剂 |
B.将尿液与试剂混合后加热至沸腾 |
丙.生成黄绿色沉淀 |
|
| ③硫酸铜 |
C.将尿液与试剂混合后微热 |
丁.生成黄色沉淀 |
|
| 戊.生成砖红色沉淀 |
试样X由氧化亚铁和氧化铜组成,取质量相等的两份试样按图所示进行实验:
(1)请写出步骤③中所发生的全部反应的离子方程式。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中氧化铜的质量为______________(用m表示)。
“探险队员”——盐酸,不小心走进了化学迷宫,迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)_____________。
(2)在不能“吃掉”盐酸的物质中,属于非电解质的是________(填写物质序号),在能“吃掉”盐酸的物质中,属于电解质的是 (填写物质序号)。
(3)如果将盐酸换成碳酸镁,它能沿着盐酸走出的路线“走出”这个迷宫吗?填“能”或“不能”_____,写出离子方程式说明其原因: 。
(4)写出氧化铝与④反应的化学方程式 ,氧化铝属于 ____________氧化物(填“酸性”“碱性”或“两性”)。
现有盐酸、铁、氢气、碳酸氢钠、氢氧化钡。根据要求回答下列问题:
(1)下图为常见物质的树状分类图:
X属于_________(填物质类属);若图中①—⑤分别代表上述五种物质,则④对应的化学式是 。
(2)上述五种物质中,有一种物质能与其他三种物质发生反应。该物质是__________。
(3)上述五种物质间发生置换反应的离子方程式____________________
(4)写出过量的③与④反应的离子方程式 ____________________