(1)25 ℃时,合成氨反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
①在该温度时,取l mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是_______92.4 kJ。(填“小于”, “大于” 或“等于”)
②一定条件下,上述可逆反应在体积固定的密闭容器中进行,下列叙述能说明反应已达到平衡的是_______________。
| A.NH3生成的速率与NH3分解的速率相等 |
B.混合气体的反应速率 v正(NH3)=v逆(H2) v正(NH3)=v逆(H2) |
| C.容器内的密度不再变化 |
| D.单位时间内消耗a mol N2,同时生成2a mol NH3 |
(2) 25 ℃时,将工业生产中产生的NH3溶于水得0.1mol/L氨水20.0 mL,测得PH=11,则该条件下,NH3•H2O的电离平衡常数为__________。向此溶液中加入少量的氯化铵固体,此时 值将_____(填“增大”, “减小” 或“不变”)。
值将_____(填“增大”, “减小” 或“不变”)。
(3)常温下,向0.001mol/LAlCl3溶液中通入NH3直至过量,当PH=_________时,开始生成沉淀(已知:Ksp[Al(OH)3]=1.0×10-33)
某新型液晶有机物基元IV的合成线路如下:
(1)Ⅰ的分子式,Ⅰ中含氧官能团的名称,反应①的类型为。
(2)CH2=CHCH2Br与NaOH水溶液反应的化学方程式。
(3)II可发生加聚反应,所得产物的结构简式。
(4)有关化合物Ⅰ和II的说法中,不正确的是。
| A.1molⅠ充分燃烧需要消耗6mol O2 | B.1molⅠ最多可消耗2mol NaOH |
| C.1mol II最多与5mol H2发生加成反应 | D.II能使酸性KMnO4溶液褪色 |
(5)一定条件下,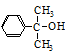 也可与III发生类似反应③的反应,生成有机物V,V的结构
也可与III发生类似反应③的反应,生成有机物V,V的结构
简式是。
(6)化合物I的同分异构体中,苯环上一溴代产物只有两种,遇FeCl3溶液显紫色,还能发
生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式。
某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]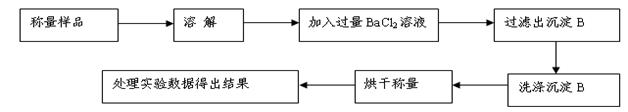
(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为。
(2)洗涤沉淀B的操作是。
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________。
方案Ⅱ.乙组同学按如下图所示装置进行实验: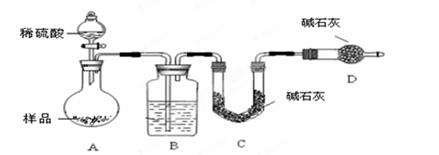
实验原理是:称量装置C吸收的CO2量来测定混合物中碳酸钠的质量分数。
主要实验流程图如下: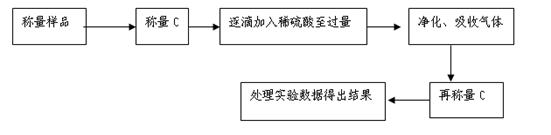
(4)该实验中装置B盛放的物质是_____________________,分液漏斗中(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(5)在C中装碱石灰来吸收净化后的气体。①样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差____________________。(填“越大”、“越小”或“不变化”)②D装置的作用是_________________________。
(6)有的同学认为为了减少实验误差,在反应前后都要通入N2(如右图),反应后通入N2的目的是______________________________。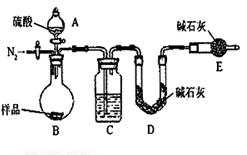
金属钒(V)在材料科学上有重要作用,被称为“合金的维生素”。在测定矿石中钒的含量时有如下操作: 用已知浓度的硫酸酸化的H2C2O4溶液,滴定(VO2)2SO4溶液。
(1)完成滴定过程的离子反应方程式,方框内填数字,短线上填物质的化学式或离子符号。
VO2+ +H2C2O4 + ______→VO2+ +CO2 + ______
(2)当收集到标准状况下气体11.2升时,电子转移的数目为
(6分) 某透明澄清溶液可能含有Na+、Fe3+、Ba2+、CO32-、SO32-、SO42-、Cl-、I-等离子中的几种,为鉴别这些离子,分别取三份少量溶液,按照以下顺序进行三个实验:
实验①:加CCl4,再滴加少量氯水,振荡后,CCl4层变为紫色;
实验②:加盐酸后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
实验③:加BaCl2溶液产生白色沉淀,过滤出沉淀,在沉淀中加入足量盐酸,沉淀不能完全溶解。
(1)分析上述3个实验,用离子符号写出每一个实验得出的结论,可不必完全填满。
实验①:含有;不含;
实验②:含有;不含;
实验③:含有;不含;(可不必完全填满)
(2)通过上述实验,不能确定是否存在的离子是。
写出下列化学方程式或离子方程式。
(1)钠与氧气在常温下反应;化学方程式____________________________________。
(2)实验室多余氯气的尾气吸收;离子方程式______________________________。
(3)漂白粉的作用原理,与H2O和CO2作用;化学方程式______________________________。
(4)氢氧化铁加热分解;化学方程式________________________。
(5)次氯酸光照分解;化学方程式____________________________________。
(6)铁丝在氯气中燃烧;化学方程式__________________________________。
(7)三氯化铁溶液与铁粉反应;离子方程式________________________。
(8)新制氢氧化亚铁遇空气被氧化成氢氧化铁;化学方程式___________________________。
(9)加热碳酸氢钙溶液产生白色沉淀;化学方程式___________________________________。
(10)碳酸氢钠溶液与氢氧化钠溶液混合;化学方程式________________________________。