已知通常状况下甲、乙、丙、丁等为气体单质,A、B、C、D、E、F、G、H等为化合物,其中A、B、E、G均为气体,C为常见液体。反应①、②、③都是重要的化工反应,反应④是重要的实验室制取气体的反应。有关的转化关系如下图所示(反应条件均已略去)。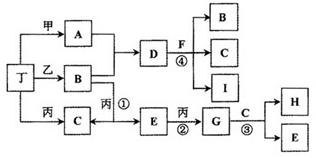
请回答下列问题:
(1)反应④的化学方程式为: ________________________。
(2)B和E在一定条件下可发生反应,这是一个具有实际意义的反应,可消除E对环境的污染,该反应氧化产物与还原产物的物质的量之比为________。
(3)0.1mol lL-1A溶液和0.1mol •L-1B溶液等体积混合,溶液呈________性,原因是(用离子方程式说明) ________________。
(4)请设计实验检验D晶体中的阳离子(简述实验操作、现象和结论):________________。
(5)pH相同的A、D、H三种溶液,由水电离出的c(OH-)的大小关系是(用A、D、H表示) : ____________。
(6)向一定量的Fe、FeO、Fe3O4的混合物中,加入1mol• L-1 A的溶液100 mL,恰好使混合物全部溶解,且放出336mL(标准状况下)的气体,向所得溶液中加入KSCN溶液,溶液无红色出现;若取同质量的Fe、FeO、Fe3O4混合物,加入1 mol • L-1 H的溶液,也恰好使混合物全部溶解,且向所得溶液中加入KSCN溶液,溶液也无红色出现,则所加入的H溶液的体积是________。
取1.43g Na2CO3·XH2O 溶于水配成10mL 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.0mL,并收集到112mL CO2(标准状况)。
计算:(1)稀盐酸物质的量浓度为;
(2)Na2CO3·xH2O的摩尔质量;
(3)x=;
(1)在1 mol Al2(SO4)3中含个SO42―。
(2)9.03×1023个氨气在标准状况下含______ L氨气。
(3)0.5mol H2SO4的质量是______g,能和______molNaOH完全反应。
(4)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量是g/mol。
已知反应:
①SO2+2NaOH=Na2SO3+H2O
②SO2+2H2S=3S↓+2H2O
③SO2+Br2+H2O=H2SO4+2HBr
(1)将③反应中的反应物和生成物化学式填入下表。(每个格子只填一种)
| 类型 |
酸性氧化物 |
电解质 |
非电解质 |
| 化学式 |
(2)从①反应后的溶液中获取Na2SO3晶体,需进行的操作是;
从②反应后的溶液中获取S单质,需进行的操作是;
从③反应中提取剩余的Br2,需进行的操作是。
请在下列化学方程式上标出该反应中电子转移的方向和数目,并指出氧化剂、还原剂。
8NH3+3Cl2 ===6NH4Cl+N2氧化剂是_________,还原剂是_________。
按要求回答下列各题:
(1)某原子质子数为16,写出该原子的结构示意图;
(2)某一价阳离子的核外电子排布与Ne相同,写出该离子的结构示意图;
(3)核内中子数为N的R2+,质量数为A,则该离子的核外电子数为。