已知:当羟基与双键碳原子相连接时,易发生如下转化: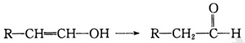 化学式为C11H10O4的有机物A有如下的转化关系
化学式为C11H10O4的有机物A有如下的转化关系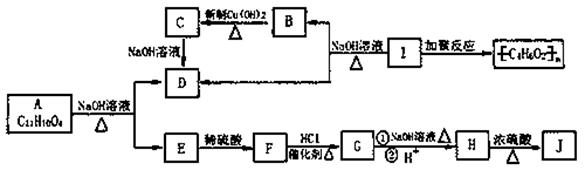
其中F为苯的二元对位取代物,分子中含有羟基、羧基及碳碳双键,存在顺反异构现象,J分子中有三十六元环状结构,其中一个六元环含有两个酯基。试回答:
(1)写出有机物结构简式:I:____ ,J:
(2)指出F→G的反应类型:
(3)写出A→E+D 的化学反应方程式:
(4)写出G与NaOH溶液共热的化学反应方程式:
(5)F的同分异构体F1也为苯的二元对位取代物,且与F具有相同的官能团,但其不存在顺反异构现象,则F1的结构简式为 。
(7分)据报道,最近摩托罗拉(MOTOROLA)公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月充电一次。假定放电过程中,甲醇完全氧化产生的CO2被充分吸收生成CO32-
(1)该电池反应的总离子方程式为;
(2)甲醇在极发生反应(填正或负),电池在放电过程中溶液的pH将(填降低或上升、不变);
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一电极通入汽油蒸气。其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2 (Zr:锆)固体,它在高温下能传导O2-离子(其中氧化反应发生完全。以丁烷(C4H10)代表汽油。
①电池的正极反应式为。
②放电时固体电解质里的O2-离子的移动方向是向极移动(填正或负)。
(13分)物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识的回答:
(1)A为0.1 mol•L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为。
(2)B为0.1 mol•L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(共3个,分别用离子方程式表示):;实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入,目的是;若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq),在25℃时,AgCl的Ksp=1.8×10-10
Ag+(aq)+Cl-(aq),在25℃时,AgCl的Ksp=1.8×10-10
25oC时,现将足量AgCl分别放入:①l00mL蒸馏水;②l00mL 0.2 mol•L-1AgNO3溶液;③100mL 0.1 mol•L-1氯化铝溶液;④100mL 0.1 mol•L-1盐酸溶液。充分搅拌后,相同温度下Ag+浓度由大到小的顺序是(填写序号);②中C1-的浓度为_ mol•L-1。
有机化合物A的相对分子质量大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。请回答:
⑴该化合物分子中含有个氧原子。
⑵该化合物的摩尔质量是。
⑶化合物化学式为。
含苯酚的工业废水处理的流程图如下图: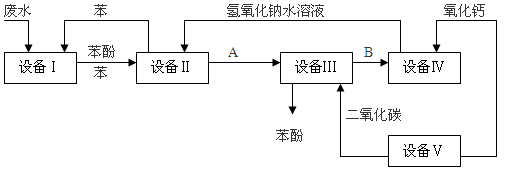
(1)上述流程里,设备Ⅰ中进行的是______操作(填写操作名称)。实验室里这一步操作可以用______进行(填写仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是______,由设备Ⅲ进入设备Ⅳ的物质B是______。
(3)在设备Ⅲ中发生反应的化学方程式为:______________________________________。(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和______。通过______操作(填写操作名称),可以使产物相互分离。
(5)上图中,能循环使用的物质是C6H6、CaO、______、______。
已知(1) (R和R’代表烃基)
(R和R’代表烃基)
(2)苯的同系物能被高锰酸钾氧化,如:
(3)
(苯胺,弱碱性,易氧化)
化合物C是制取消炎灵(盐酸祛炎痛)的中间产物,其合成路线为:
请回答下列问题:
(1)写出反应④的主要产物中含有官能团(除苯环外)的结构简式_____________。
(2)B物质的结构简式是_____________。
(3)反应①②的化学方程式
①_______________________________________,
②_______________________________________。
(4)反应①~⑤中,属于取代反应的是(填反应序号)_____________。