某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验I:制取NaClO2晶体
己知:NaClO2饱和溶液在温度低于38℃时析出品体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。利用下图所示装置进行实验。
(1)装置③的作用是
装置①的作用是
(2)装置②中产生ClO2的还原剂是
装置④中制备ClO2的化学方程式为
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶:②趁热过滤;③ ;④低于60℃干燥,得到成品。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:
①准确称取所得亚氯酸钠样品小打烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-)。
(4)达到滴定终点时的现象为
(5)该样品中NaClO2的质量分数为 (用含m、c、V的代数式表示)。
(6)在滴定操作正确无误的情况下,此实验测得结果偏高,原因用离子方程式表示为 。
有如图电解装置,图中A装置中盛1 L 2 mol· L—1AgNO3溶液,B装置中盛1L 2 mol·L—1Na2SO4溶液。通电后,湿润的KI淀粉试纸的C端变蓝色,电解一段时间后,试回答: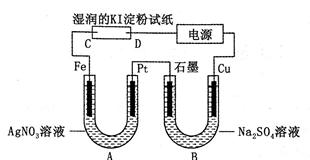
(1)A中发生反应的化学方程式为___________________________________________。
(2)在B装置中观察到的现象是____________________________________________。
(3)室温下,若从电解开始到时间为T时,A、B装置中共收集到气体0.168L(标准状况),若电解过程中无其他副反应发生,且溶液体积变化忽略不计。试计算:T时刻A装置溶液中c(H+)(写出计算过程)。
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢材年产量的四分之一。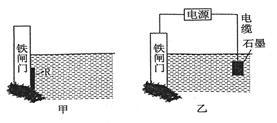
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为________________
(2)为了降低某铁闸门被腐蚀的速率,可以采用上述图甲所示的方案,其中焊接在铁闸门上的固定材料R可以采用____(填序号)。
| A.铜 | B.钠 | C.锌 | D.石墨 |
(3)上图乙所示的方案也可以降抵铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的_______极。
现有NH4Cl和氨水组成的混合溶液。请回答下列问题(填“>”、“<”或“=”):
(1)若溶液的pH=7,则该溶液中c(NH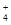 )_________c (Cl—)。
)_________c (Cl—)。
(2)若溶液的pH>7,则该溶液中c(NH+)_________c(Cl—)。
(3)若c(NH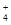 )<c (Cl—),则溶液的pH__________7。
)<c (Cl—),则溶液的pH__________7。
在一体积为10L的密闭客器中,通入一定量的CO和H2O,在85℃发生如下反应:
CO (g)+H2O(g) 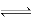 CO2(g)+H2(g)△H<O。
CO2(g)+H2(g)△H<O。
CO和H2O浓度变化如图所示: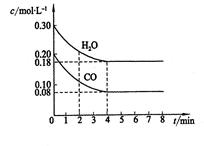
请回答下列问题:
(1)能判断该反应达到化学平衡状态的依据是___________________(填选项序号)。
a.容器中压强不变
b.混合气体中c(CO)不变
c.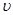 正(H2)=
正(H2)= 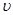 逆(H2O)
逆(H2O)
d.c(CO2)=c(CO)
e.容器中气体密度不变
f.1 mol H-H键断裂的同时断裂2 mol H-O键
(2)①0~4min内的平均反应速率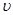 (CO)=___________mol·L—1·min—1;
(CO)=___________mol·L—1·min—1;
②85℃时,该反应化学平衡常数K=____________。
(3)85℃时,若起始时向该容器中充入1.0 molCO、3.0 molH2O,则此时CO的平衡转化率为______________。
(1)某温度下,纯水的[H+] =2.0×l0-7mol·L—l,则此时的[OH—]=__________。若温度不变,滴入稀硫酸使[H+] =5.0×l0-7mol·L—l.则[OH—]=_________,由水电离出的[H+]=__________。
(2)若l00℃时纯水电离出的[H+]为l.0×l0-6mol·L—l,此时Kw=__________。