氮化钠和氢化钠与水反应的化学方程式如下:Na3N + 3H2O=3NaOH + NH3,NaH + H2O=NaOH + H2↑。有关Na3N和NaH的叙述正确的是
| A.离子半径:Na+>N3->H+ |
| B.与水反应都是氧化还原反应 |
| C.与盐酸反应都只生成一种盐 |
| D.加热熔化时,都只破坏离子键 |
下列物质可以通过化合反应制得的是
①FeCl3 ②FeCl2 ③CuS ④FeS ⑤Fe(OH)3
| A.①②④⑤ | B.①②③④⑤ | C.①④ | D.①④⑤ |
以下能代表将NaOH溶液逐滴滴入到AlCl3与MgCl2的混合液中的图像是(图中纵坐标表示生成沉淀的质量,横坐标表示加入物质的物质的量)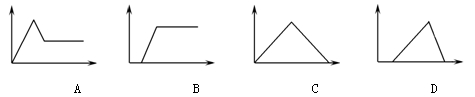
将15g金属混合物粉末投入足量稀H2SO4中,充分反应后得到11.2L H2 (在标准状况下),此金属混合物可能组成是
| A.Zn、Ag | B.Cu、Fe | C.Al、Fe | D.Mg、Al |
关于合金的叙述:①合金中至少含两种金属;②合金中的元素以化合物的形式存在;③合金中一定含金属;④合金一定是混合物。其中正确的是
| A.①②③④ | B.①③④ | C.②③④ | D.③④ |
下列金属中,既属于有色金属又属于轻金属的是
| A.铁 | B.铬 | C.钠 | D.银 |