下列各图所示实验设计能达到相应实验目的的是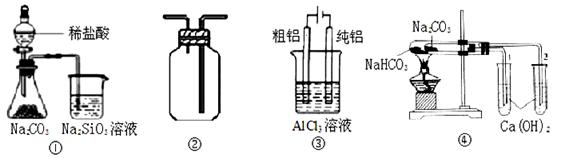
| A.用图①装置验证氯、碳、硅元素非金属性 |
| B.用图②装置能收集O2、CO2和H2 |
| C.用图③装置电解精炼铝 |
| D.用图④装置验证NaHCO3和Na2CO3的热稳定性 |
用36.5%的浓盐酸(密度1.2 g·cm-3)配1 mol·L-1的稀盐酸 100 mL,配制过程需用到哪些仪器,且先后顺序正确的是①100 mL量筒②10 mL量筒③50 mL 烧杯④托盘天平⑤100 mL容量瓶⑥胶头滴管⑦玻璃棒
| A.①③⑤⑥⑦ | B.②③⑦⑤⑥ | C.③⑤⑦⑥① | D.④③⑦⑤⑥ |
设NA是阿伏加德罗常数的数值。下列说法正确的是
| A.0.1mol·L-1的NaCl溶液中,Na+的数目为0.1NA |
| B.23 g 金属钠在常温的空气中充分氧化和在氧气中完全燃烧转移电子的数目均为NA |
| C.7.8g Na2O2中含有的阴、阳离子数目均为0.1NA |
| D.标准状况下,22.4L水中分子个数为NA |
下列说法正确的是
| A.酸式盐的水溶液一定显酸性 |
| B.酸性氧化物一定是非金属氧化物 |
| C.丁达尔效应是溶液和胶体的本质区别 |
| D.HClO是弱酸,但NaClO是强电解质 |
分类是化学学习与研究的常用方法,下列分类正确的是
| A.Na2O2、MgO、Al2O3均属于碱性氧化物 |
| B.纯碱、烧碱、熟石灰均属于碱 |
| C.酸、碱、盐之间发生的反应均属于复分解反应 |
| D.混合物、分散系、胶体从属关系如图所示 |

为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性
②取少量溶液中入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体
③在上述溶液中再滴加Ba(NO3) 3溶液,产生白色沉淀
④取上层清液继续滴加Ba(NO3) 3溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀
根据实验以下推测正确的是 ()
| A.一定有SO32-离子 | B.一定有CO32-离子 |
| C.Cl-离子一定存在 | D.不能确定HCO3-离子是否存在 |