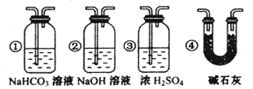
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸
点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。
某学生拟用左下图所示装置模拟工业制取并收集ClO2。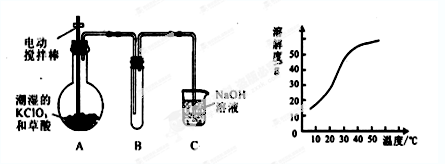
(1)A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式: 。
(2)A必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有 、 ;
(3)反应后在装置C中可得NaClO2溶液。已知NaClO2饱和溶液中在温度低于38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2。根据上图所示的NaClO2的溶解度曲线,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
① ;② ;③洗涤;④干燥。
(4)ClO2很不稳定,需随用随制,用水吸收得到ClO2溶液。为测定所得溶液中
ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10 mL,稀释成100 mL试样;量取V1mL试样加入到锥
形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;此时发生的离子方程式
为: ;
步骤3:加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。
则原ClO2溶液的浓度为 g/L(用含字母的代数式表示)。
(已知2 Na2S2O3+I2= Na2S4O6+2NaI)
动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
| 实验步骤 |
实验现象 |
||||
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
|
||||
| ⑤将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
||||
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究 递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。
仪器: ① ,② ,烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号)(各1分)
| 实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 实验现象(填A~F) |
写出步骤②中发生的化学方式: ,
写出步骤⑥中发生的离子方式: ,
此实验的结论:
某课外活动小组利用下图装置探究SO2与Na2O2的反应。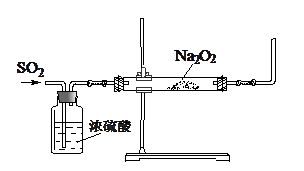
(1)请指出该装置中一个不合理的地方:。
(2)第1小组同学认为Na2O2与SO2反应类似CO2与Na2O2的反应,该反应的化学方程式为。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。他们作出这个推断的理由是。
(4)第3小组在通入过量SO2后,请你完成对反应完毕后硬质玻璃管中的固体成分的探究。
限选用的试剂:蒸馏水、稀盐酸、稀硫酸、稀硝酸、浓盐酸、浓硫酸、浓硝酸、Ba(NO3)2溶液、BaCl2溶液、1moL·L-1NaOH、0.01mol·L-1KMnO4、紫色石蕊试液。
①提出对玻璃管中固体成分的合理假设:
假设Ⅰ:全部为Na2SO3;
假设Ⅱ:为Na2SO3和Na2SO4的混合物;
假设Ⅲ:;
②设计实验方案(不要在答题卡上作答)。
③实验过程
根据②的实验方案,请在答题卡上写出实验步骤以及预期现象和结论。
| 实验步骤 |
预期现象和结论 |
| 步骤1:用药匙取少量固体于试管中,加入适量蒸馏水充分溶解后,将所得溶液分置于A、B试管中。 |
|
| 步骤2: |
|
| 步骤3: |
(1)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO  2CO2+N2
2CO2+N2
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
| 实验编号 |
T/℃ |
NO初始浓度 mol·L-1 |
CO初始浓度 mol·L-1 |
催化剂的比表面积 ㎡·g-1 |
| Ⅰ |
280 |
1.2×10-3 |
5.8×10-3 |
82 |
| Ⅱ |
124 |
|||
| Ⅲ |
350 |
124 |
①请在表格中填入剩余的实验条件数据。
②设计实验Ⅱ、Ⅲ的目的是。
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质。某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程。提供的装置:
步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是:(填装置序号)。
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
分析表中数据,实验室制NH3产率最高的是(填序号),其它组合NH3产率不高的原因是。
步骤二、模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置: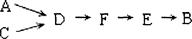
①A中反应的离子方程式:。
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:。
③D装置中的液体可换成(填序号)。
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是:。
(15分)某小组想验证Mg与二氧化碳的反应。请从下图中选用装置(可重复使用)进行该实验。现提供浓硫酸、稀盐酸、稀硫酸、镁粉、大理石、澄清的石灰水、饱和的NaHCO3溶液、饱和的Na2CO3溶液(加热的仪器已略去)。
(1)请将所选用的装置按连接顺序从上到下依次填入表格中,并写出应加入的试剂(可不填满)
| 选用的装置(填序号) |
加入的试剂 |
(2)A中发生反应的离子方程式为______________________________________,
(3)组装好装置,检查气密性良好后,加入药品,在加热C之前应进行的操作和目的是
____________________________________________________________,
(4)反应中C装置中观察到的主要现象是_____________________________。
(16分)某化学研究小组为证明CO具有还原性,首先查阅相关资料,获取下列信息:
① ;
;
②CO和H2都可在加热条件下与CuO反应;
③CO有剧毒,在空气 中可以燃烧。
中可以燃烧。
根据以上信息和有关知识,他们设计了如图所示的实验装置。
试回答下列问题:
(1)装置A中反应的离子方程式是______________。
(2)装置B.中最适宜的试剂是_______;必须用装 置C吸收气体中水蒸气的理由是_
置C吸收气体中水蒸气的理由是_ ______。
______。
(3)按照如图装置进行实验时,首先应进行的操作是检查气密性,并要排净整套装置中的空气,则排净装置中空气的必要性是______
(4)根据该实验中的_______现象,可证明CO具有还原性,有关反应的化学方程式为______________。
(5)若要根据装置F中石灰水变浑浊的现象确认CO具有还原性,则应在上图装置_______与_______之间连接右图中的_______装置(填序号)。