根据侯德榜制碱法原理,实验室制备纯碱(Na2CO3)的主要步骤是::将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质,经过处理后,转入蒸发皿中,灼烧2小时,得Na2CO3固体。
四种盐在不同温度下的溶解度(g)表
 温度 温度 溶解度 盐 |
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
60℃ |
100℃ |
| NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
39.8 |
| NH4HCO3 |
11.9 |
15.8 |
21.0 |
27.0 |
① |
—— |
—— |
—— |
| NaHCO3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
16.4 |
—— |
| NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.3 |
77.3 |
|
已知:1、①温度高于35℃NH4HCO3会分解。
2、碳酸氢钠受热分解:2 NaHCO3= Na2CO3+H2O+CO2↑某同学在查阅资料时得知:市售纯碱样品常混有氯化钠杂质。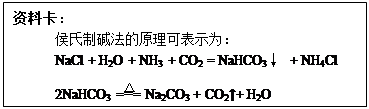
该同学设计了如下图中的装置进行实验,测定市售纯碱样品中碳酸钠的质量分数。(水蒸气的影响忽略不计,夹持装置已略去)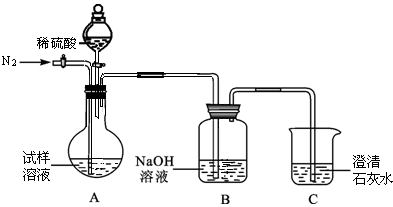
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②称量5.5 g市售纯碱样品放入烧瓶中,加适量蒸馏水溶解,得到试样溶液;
③从分液漏斗滴入稀硫酸,直到不再产生气体时为止;
④缓缓鼓入一定量的N2;
⑤称量B瓶及溶液的质量,发现增重2.2 g。
请回答下列问题:
(1)写出A中发生反应的化学方程式。
(2)鼓入一定量的N2的目的是。装置C中澄清石灰水的作用是。
(3)如果将分液漏斗中的稀硫酸换成浓盐酸,测试的结果(填偏高、偏低或不变)。
(4)该样品中碳酸钠的质量分数为%(结果保留到小数点后一位)。
(5)若用与上述实验反应原理不同的实验来测定纯碱样品中碳酸钠的质量分数,请用化学方程式表示实验原理。
黄铜是由铜和锌所组成的合金,用途广泛。某兴趣小组为探究黄铜合金的组成,取20.00 g粉末状黄铜合金样品,把60.00 g稀硫酸平均分成三等份,分三次加入样品中,均有气体产生,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 第一次 |
第二次 |
第三次 |
|
| 剩余固体的质量/g |
16.75 |
13.50 |
12.40 |
请计算:(要求写出计算过程)
(1)该黄铜合金中,锌元素的质量分数。
(2)第二次实验中放出气体的质量。
(3)向三次实验后所得混合溶液中滴加BaCl2溶液,生成不溶于水的BaSO4白色沉淀。所得沉淀的质量与BaCl2溶液质量的关系如右图所示,求所用BaCl2溶液的溶质质量分数。 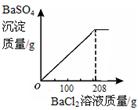
某种维生素C药品说明书的部分信息如右图。试计算:(要求写出计算过程)
(1)维生素C的相对分子质量。
(2)维生素C中所含碳、氢、氧元素的质量比。
(3)某病人每天服用该药品3次,则他每天通过服药摄入Vc的质量。
在化学实验技能考试做完“二氧化碳的制取和性质”实验后,废液桶中有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。为避免污染环境并回收利用废液,化学兴趣小组做了如下实验:取废液10kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液pH与加入的碳酸钠溶液的质量关系如右图所示(已知:Na2CO3+CaCl2=CaCO3↓+2NaCl):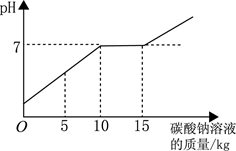
(1)通过右图可知,当碳酸钠溶液质量加到kg时,废液恰好处理完(盐酸与氯化钙的混合溶液完全转化成氯化钠溶液)。
(2)计算废液中氯化钙的质量分数。
(3分) 登山队员常用的能源是氢化钙(CaH2)固体,它和水反应生成氢氧化钙和氢气(CaH2 + 2H2OCa(OH)2 + 2H2↑),氢气供燃烧之需。现有840 g氢化钙固体,与足量水反应可生成氢气多少克?