从能量的变化和反应的快慢等角度研究反应: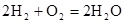 。
。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
| A.使用催化剂 | B.适当提高氧气的浓度 |
| C.适当提高反应的温度 | D.适当降低反应的温度 |
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是________。
(3)从断键和成键的角度分析上述反应中能量的变化。
【资料】①键能:拆开1mol化学键需要吸收的能量,或是形成1mol化学键所放出的能量称为键能。
②化学键的键能:
| 化学键 |
H—H |
O=O |
H—O |
键能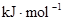 |
436 |
496 |
463 |
请填写下表:
| 化学键 |
填“吸收热量” 或“放出热量” |
能量变化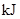 |
|
| 拆开化学键 |
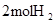 中的化学键 中的化学键 |
_______________ |
_______________ |
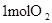 中的化学键 中的化学键 |
|||
| 形成化学键 |
 键 键 |
_______________ |
_______________ |
| 总能量变化 |
_______________ |
_______________ |
(4)氢氧燃料电池的总反应方程式为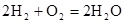 。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
(1)某肉制品包装上印有相关配料:精选瘦肉、食盐、胭脂红、苯甲酸钠。其中属于调味剂的是,属于着色剂的是,属于防腐剂的是。
(2)亚硝酸钠有毒,其外观和咸味与食盐很相似,因此要防止因误食亚硝酸钠而发生事故。亚硝酸钠和氯化钠的部分性质如下表:
| 性质 |
亚硝酸钠 |
氯化钠 |
| 1.酸性条件下的稳定性 |
微热时分解为NO和NO2 |
微热时不分解 |
| 2.熔点 |
271℃ |
801℃ |
| 3.室温时的溶解度 |
约80g |
约35g |
①请根据表中信息设计一种鉴别NaNO2和NaCl的方法,写出简单的操作过程、现象和结论:
②碘是人体中不可缺少的(选填“常量”或“微量”)元素。
③食盐中加入碘元素能有效防止缺碘引起的疾病。以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%。现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%。食盐中加入碘化钾的碘损失率高的原因是;(填字母)。
a.碘化钾被氧化,造成碘化钾的碘损失率高。 b.碘化钾升华,造成碘化钾的碘损失率高。
c.碘化钾与食物中的成分发生反应,造成碘化钾的碘损失率高。
④萃取碘水中的碘时,一般选用的试剂是(填字母);
A.酒精 B.四氯化碳 C.乙酸
⑤可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾。反应化学方程式为:
5KI+KIO3 + 6HCl ="=" 6KCl + 3I2 + 3H2O,反应的现象是
⑥已知碘酸钾受热易分解,你认为在用碘酸钾加碘盐进行烹饪时应注意什么问题?。
⑶糖类、油脂、蛋白质都是人体必需的营养物质。
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和 ________(写结构简式)。人体中共有二十多种氨基酸,其中人体自身_____(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
③淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:。
已知NO2和N2O4可以相互转化:2NO2(g)  N2O4(g)△H<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。
N2O4(g)△H<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。
(1)图中共有两条曲线X和Y,其中表示NO2浓度随时间变化的曲线是;a、b、c、d四个点中,表示化学反应处于平衡状态的点是。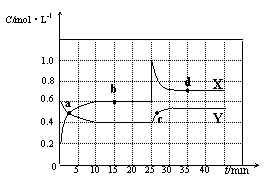
(2)①前10 min内用NO2表示的化学反应速率v(NO2)=mol·L-1·min-1。
②反应2NO2(g)  N2O4(g)在b点的平衡常数K(b)=。
N2O4(g)在b点的平衡常数K(b)=。
③反应2NO2(g)  N2O4(g)在d点的平衡常数K(d)与b点的平衡常数K(b)的关系:
N2O4(g)在d点的平衡常数K(d)与b点的平衡常数K(b)的关系:
K(d)K(b)(填“>”、“=”或“<”)。
(3)①据图分析,在25 min时采取的措施是(填序号)。
| A.加入催化剂 | B.缩小容器体积 |
| C.加入一定量的NO2 | D.加入一定量的N2O4 |
②若在35 min时,保持温度不变,快速缩小容器的体积至1 L,气体的颜色变化过程是
在25℃时,用石墨电极电解2.0L,2.5 mol/LCuSO4溶液。5 min后,在一个石墨电极上有6.4gCu生成。试回答下列问题:
(1)极发生氧化反应(填阴,阳),电极反应式为。
(2)极发生还原反应(填阴,阳),电极反应式为。
(3)有mol电子发生转移,得到氧气的体积(标准状况)是L,溶液的pH是。反应速率v(Cu2+):v(O2)==
(4)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差g,电解液的pH(填“变小”、“变大”或“不变”)
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
(1)a极是极,b极是极,
电极反应式分别为,。
(2)氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料,往往是某些碳氢化合物,如甲烷(天然气)、汽油等。请写出将图中H2换成CH4时所构成的甲烷燃料电池中a极的电极反应式:。此时电池内总的反应方程式为。
已知难溶于水的盐在水中存在溶解平衡: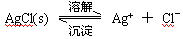
在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 KSP表示:KSP= c(Ag+)·c(Cl-)=1.8·10-10。
若把足量AgCl分别放入① 100 mL蒸馏水,② 100 mL 0.1 mol / L NaCl溶液,③ 100 mL 0.1 mol / L AlCl3溶液,④ 100 mL 0.1 mol / L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是 ______>______>______>______。在0.1 mol / L AlCl3溶液中,Ag+的物质的量浓度最多为_________mol / L。