某溶液中仅含下表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol。
| 阴离子 |
SO42-、NO3-、Cl- |
| 阳离子 |
Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
①若向原溶液中加入KSCN溶液,无明显变化。②若向原溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变。③若向溶液中加入BaCl2溶液,有白色沉淀生成试回答下列问题。
(1)若先向原溶液中加入过量的盐酸,再加入KSCN溶液,现象是 。
(2)原溶液中含有的阳离子是 。
(3)向原溶液中加入足量的盐酸,发生反应的离子方程式为 。
(4)向原溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体用托盘天平称量质量为 。
(12分) 已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下 表。
表。
| 元素 |
结构或性质信息 |
| X |
原子的L层上s电子数等于p电子数。 |
| Y |
原子核外的L层有3个未成对电子。 |
| Z |
在元素周期表的各元素中电负性仅小于氟。 |
| Q |
单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
| R |
核电荷数是Y与Q的核电荷数之和 |
| E |
原子序数比R大3 |
请根据信息回答有关问题:
(1)元素Y的原子核外 共有种不同运动状态的电子,有种不同能级的电子。
共有种不同运动状态的电子,有种不同能级的电子。
(2)X、Y、Z三种元素的电负性由高到低的排列次序依次为(写元素符号)。
(3)X、Z、Q元素均表现最低化合价时的三种氢化 物中,沸点由高到低
物中,沸点由高到低 的排列次序依次为(写化学式)。
的排列次序依次为(写化学式)。
(4)R的最高化合价为。R的一种配合物的化学式为RCl3·6H2O。已知0.01 molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是。
A.[R(H2O)6]C l3 B.[R(H2O)5Cl]Cl2·H2O
l3 B.[R(H2O)5Cl]Cl2·H2O
C. [R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(5)元素E能形成八面体构型的配合物离子[E (YH3) x Q 2]+,则中心离子为(写化学式),配位体为(写化学式),x 的值为。
(6)Y的最低价氢化物与Z的一种氢化物反应,生成的两种产物均不 污染环境,其反应的化学方程式为。
污染环境,其反应的化学方程式为。
下表是元素周期表的一部分,表中所列字母分别代表一种化学元素: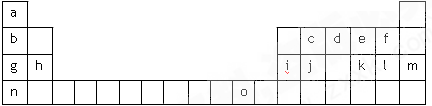

试回答下列问题:
(1 )
) 按电子排布,可把周期表中的元素划分成5个区,其中j位于区。
按电子排布,可把周期表中的元素划分成5个区,其中j位于区。
(2)请写出字母o代表的元素的基态原子外围电子排布式。
(3)第三周期8种元素按单质熔点高低的顺序如图,其中 序号“8”代表(填元素符号);其中电负性最大的是(填右图中的序号),第一电离能最大的是(填图中的序号)。
序号“8”代表(填元素符号);其中电负性最大的是(填右图中的序号),第一电离能最大的是(填图中的序号)。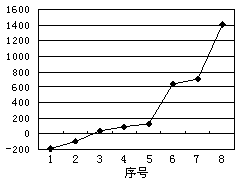
(4)由j原子跟c原子以1∶1相互交替结合而形成的晶体,晶体类型与晶体j相同。两者相比熔点更高的是(填化学式),试从结构角度加以解释:
。
(5)COCl2俗称光气,分子中C原子采取杂化方式成键;分子中的共价键含有(填标号)。
a.2个σ键 b.2个π键 c.1个σ键、2个π键 d.3个σ键、1 个π键
个π键
(6)已知[Ni(NH3)2Cl2]可以形成A、B两种固体,则[Ni(NH3)2Cl2] 分子的空间构型
是。若A在水中溶解度较大,B在CCl4中溶解度较大,试画出A分子的几何构型图。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成配位数为6的配合物F,且两种配体的物质的量之比为2∶1,三个氯离子位于外 界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小 到大的顺序为。
到大的顺序为。
(2)B的氢化物的分子空间构型是。其中心原子采取杂化。
(3)写出化合物AC2的结构式;一种由B、C组成的化合物与AC2互为等电子体,其化学式为。
(4)E的核外电子排布式是,配合物F的化学 式为。
式为。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是。
(6)B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高的原因是:
。
m、n、x、y四种主族元素在周期表里的相对位置如下图所示。已知它们的原子序数总和为46,则: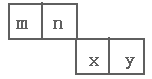
(1)写出n元素基态原子电子排布图:。
(2)元素x气态氢化物的分子式为,空间构型为。
(3)m与y所形成的化合物含键,属分子。(填“极性”或“非极性”)
(4)x位于周期表的第周期,第族;其原子结构示意图为。
(5)由n、y的氢化物相互作用所生成的物质的电子式为,此物质属于化合物。(填“离子”或“共价”)
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40—500C时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生反应是2Cu+ = Cu2+ + Cu,。根据以上信息,结合自己所掌握的化学知识,回答:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是。
(2)写出CuH在氯气中燃烧的化学反应方程式
(3)CuH溶解在稀盐酸中生成的气体是,如果反应中生成了标况下22.4 L的气体,被还原的离子得电子的物质的量是。