重金属盐可使人中毒。当人误食重金属盐时,可以喝 解毒。原因是上述食品中含有较多的 ,可以跟重金属盐形成不溶于水的化合物,可以减轻重金属盐类对胃肠黏膜的危害,起到缓解毒性的作用。
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化: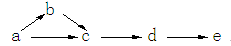
其中:a是单质;b是气体且为含氢化合物;c、d是氧化物;e是最高价含氧酸。
(1)如果a是一种淡黄色粉末固体,试推断:(用化学式表示):
a;b;e。写出由c生成d的化学方程式____________________________
(2)如果a为单质且是一种常见气体,试推断这五种物质(用化学式表示):
a;b;c;并写出由d生成e的化学方程式________________________
有机物A(分子式C6H10O3)是合成某种隐形眼镜材料的单体,A可发生如下变化: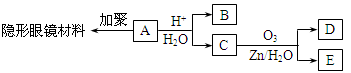
已知:Ⅰ.物质B是最简单的二元醇,已知两个羟基连在同一个碳上不稳定;物质D不能发生银镜反应,但能与NaHCO3溶液反应放出气体。
Ⅱ.
回答下列问题:
(1)隐形眼镜材料的结构简式为;
(2)写出物质B在铜催化下与O2反应的化学方程式;
(3)与C互为同分异构体,分子为链状的酯类物质共有种;
对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。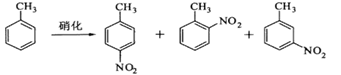
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是。
(2)滤液在分液漏斗中洗涤静置后,有机层处于层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
| 催化剂 |
n(催化剂) n(甲苯) |
硝化产物中各种异构体质量分数(%) |
总产率(%) |
||
| 对硝基甲苯 |
邻硝基甲苯 |
间硝基甲苯 |
|||
| 浓H2SO4 |
1.0 |
35.6 |
60.2 |
4.2 |
98.0 |
| 1.2 |
36.5 |
59.5 |
4.0 |
99.8 |
|
| NaHSO4 |
0.15 |
44.6 |
55.1 |
0.3 |
98.9 |
| 0.25 |
46.3 |
52.8 |
0.9 |
99.9 |
|
| 0.32 |
47.9 |
51.8 |
0.3 |
99.9 |
|
| 0.36 |
45.2 |
54.2 |
0.6 |
99.9 |
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有。
已知一氧化碳与水蒸气的反应为
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
在密闭容器中,将1.0mol CO与3.6mol H2O混合加热到434℃,在434℃的平衡常数K1=9,
(1)我们跟踪测定H2O的物质的量浓度,如图所示: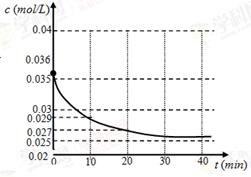
则0~20min的反应速率是________
(2)从434℃升温至800℃,800℃的平衡常数K2=1,则正反应为_____________(填“放热反应”或“吸热反应”或“不能确定”)。
(3)求800℃平衡时CO转化为CO2的转化率(写出必要的计算过程)。
在我校食堂南侧的绿树青草间,有一由井水形成的弯弯小溪。近来发现,昔日那碧波澄清的水面上,泛起了棕红色的“水锈”,小煞风景。
(1)根据学过的知识,你认为该“水锈”的主要成分可能是(写化学式)。
(2)怎样用化学方法检验此“水锈”的主要成分?简述实验操作:
第一步:取含“水锈”的混浊液少许于试管;
第二步:;
第三步:。
上述有关反应的离子方程式为、。