I(1)在淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,反应的离子方程式是 。
(2)在碘和淀粉形成的蓝色溶液中通入SO2气体,发现蓝色逐渐消失,反应的离子方程是 。
(3)对比(1)和(2)实验所得的结果,将Cl 、I
、I SO2按还原性由强到弱顺序排列为 。
SO2按还原性由强到弱顺序排列为 。
II (4) 除去铁粉中混有铝粉的试剂是 ,离子方程式为
(5) 1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
煤化工中两个重要反应为①C(s)+H2O(g)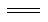 H2(g)+CO(g)ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g)
H2(g)+CO(g)ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g) CO2(g)+ H2(g)。
CO2(g)+ H2(g)。
(1)下列说法正确的是 。
| A.当反应①的容器中混合气体的密度不再变化时反应达到最大限度 |
| B.反应②的熵变△S>0 |
| C.反应①中增加C固体的量能增大反应速率 |
| D.在反应中②及时分离出产生的H2对正反应速率无影响 |
(2)若工业上要增加反应①的速率,最经济的措施为 。
(3)现将不同量的CO(g)和H2O(g)分别通入2L恒容密闭容器中进行反应,得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所 需时间/ min |
||
| CO |
H2O |
H2 |
CO2 |
|||
| I |
650 |
4 |
2 |
1.6 |
1.6 |
5 |
| Ⅱ |
900 |
2 |
1 |
0.5 |
0.5 |
3 |
| Ⅲ |
900 |
a |
b |
c |
d |
t |
①实验I中,从反应开始到反应达到平衡时,H2O的平均反应速率为___。
②CO(g)和H2O(g)反应的△H 0(填“大于”、“小于”或“等于”)
③实验III中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是______,与实验Ⅱ相比,化学平衡常数 (填“增大”、“减小”或“不变”)。
④若在900℃时,实验II反应达到平衡后,向此容器中再加入1 mol CO、0.5 mol H2O、0.2 mol CO2、0.5 mol H2,平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)。
(4)CO、H2可用于甲醇和甲醚,其反应为(m、n均大于0):
反应①:CO(g)+2H2(g) CH3OH(g)ΔH= -mkJ·mol-1
CH3OH(g)ΔH= -mkJ·mol-1
反应②: 2CO(g)+4 H2(g) CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
反应③:2CH3OH(g) CH3OCH3(g)+ H2O(g)△H<0
CH3OCH3(g)+ H2O(g)△H<0
则m与n的关系为 。
下图是以A为原料合成一种高分子材料G的流程图。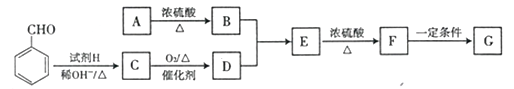
已知:
①A的分子式为C2H6O2
②G的结构简式为: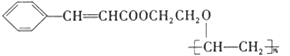
③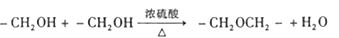
④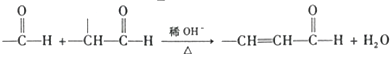
请回答下列问题:
(1)A的名称是: F→G的反应类型是
(2)B的核磁共振氢谱上共有 个吸收峰;
(3)C的结构简式是 ;
(4)A→B的化学方程式是_______,B+D→E的化学方程式是 ;
(5)写出同时满足下列条件的D的所有同分异构体的结构简式: 。
①属于酯类且苯环上只有一个取代基
②除苯环外不再含其他环状结构
化合物A是天然蛋白质水解的最终产物,其相对分子质量为165,其中O元素的质量分数小于20%,N元素的质量分数小于10%。
请回答下列问题:
(1)A的分子式为 ;
(2)光谱测定显示,A分子结构中含有苯环且不存在甲基(一C H3),则A的结构简式为 ;
(3)写出A发生缩聚反应的化学方程式 。
下图A一G是几种烃的分子球棍模型: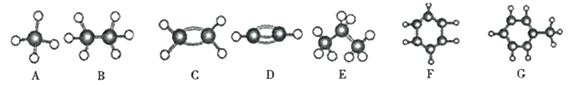
请回答下列问题:
(l)含氢量最高且常温下为气态的烃是(填对应字母) ;
(2)一卤代物种类最多的是(填对应字母) ;
(3)A一G在充有足量氧气的密闭恒容容器中完全燃烧,150℃时测得燃烧前后的压强不变的有 (填对应字母);
(4)写出实验室制取D的化学方程式 。
X、Y、Z、W、R均为前四周期元素且原子序数依次增大,X的基态原子核外有7种不同运动状态的电子,Y原子最外层有2对成对电子,Z的原子序数为Y的原子序数的2倍,W3+的基态离子的3d轨道为半充满状态,新制备的R的氢氧化物悬浊液可用于检验醛基的存在。请回答下列问题:
(1)X2分子中σ键和π键数目比是 ;
(2)R的晶胞结构如图所示,该晶胞中所含的原子个数是 ;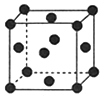
(3)下列有关X、Y、W的说法正确的是 ;
①第一电离能的排序是Y>X>W
②常温下,Y的氢化物分子间存在氢键
③XY3一中X的杂化轨道类型为sp3杂化
④W属于d区的元素
(4)X的气态氢化物分子的空间构型为 ,将其水溶液滴入R的氢氧化物悬浊液中,反应的离子方程式为 ;
(5)将Na2Y2与W2+的硫酸盐按物质的量之比为1:1混合并投入水中,溶液中出现红褐色沉淀并有无色气体产生,该反应的离子方程式是 。