镁在高温下与O2、N2或CO2均可以发生反应,试解决下列问题。
(1)工业通常采用电解熔融氯化镁冶炼金属镁,不以氧化镁为原料的理由是 。
(2)将燃着的镁条伸入盛满CO2的集气瓶中,镁条剧烈燃烧,发出耀眼的白光,瓶内壁上有黑色物质生成,化学方程式为 。
(3)由金红石(TiO2)制取单质钛(Ti),涉及到的反应步骤为
金属镁的作用为 ,在Ar气氛中的进行的理由是 。
(4)现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知:
Mg+H2O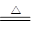 MgO+H2↑ Mg3N2 +6H2O =3Mg(OH)2+2NH3↑
MgO+H2↑ Mg3N2 +6H2O =3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示。

①导管口间的连接次序是:a →( )()→()()→()()→ h
②通气后,应先点燃 (填“B”或“C”)装置的酒精灯,装置A的作用是 ,装置E的作用是 。
③请设计一个简单的小实验验证产物是氮化镁 。
Ⅰ、Na2O2与SO3(g)的反应类似于Na2O2与CO2(g)的反应,请写出Na2O2与SO3反应的化学方程式:。
Ⅱ、某学生课外活动小组模拟呼吸面具中的反应原理,设计用下图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。
实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。
请回答:
(1)图中各装置接口连接顺序是(填各接口的编号,其中连接胶管及夹持装置均省略,):→→→⑥ → ⑦ →→→
(2)装置C中放入的反应物是和(填化学式)。
(3)装置B的作用是。
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意__a___和(填字母编号)。
| A.视线与凹液面最低处相平 | B.等待气体恢复常温才读数 |
| C.读数时应上下移动乙管,使甲乙两管液面相平 | D.读数时不一定使甲乙两管液面相平 |
(5)实验测得收集的氧气在标准状况下体积为V L,则参与反应的Na2O2的物质的量为mol。
实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液250 mL:
(1)配制溶液时,一般可以分为以下几个步骤:(完成下列空格)
A.计算 B.称量 C. D. E.F.定容 G.摇匀、装瓶
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、量筒、还有______ __
使用容量瓶前必须进行的一步操作是________.
(3)需称量________g烧碱固体,固体应该放在________中称量。
(4)定容时的操作应为用玻璃棒引流加入蒸馏水,至液面离刻度线约__________,改用______ _滴加至凹液面下沿与刻度线相平。
(5)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是________.(双选)
A.没有洗涤烧杯和玻璃棒 B.转移溶液时不慎有少量洒到容量瓶外面
C.容量瓶不干燥,含有少量蒸馏水 D.定容时俯视刻度线
E.未冷却到室温就将溶液转移到容量瓶并定容
(6)若从所配制溶液取出100 mL ,则这100 mL溶液的物质的量浓度为__________________,
若再将这100 mL溶液加水稀释成1 L的溶液,则稀释后所得溶液的物质的量浓度为____________________。
(本题16分)为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和甲中加热装置已略,气密性已检验)。
实验步骤:
1.在甲装置中,打开活塞a,加热,待装置中充满黄绿色气体时,与丙装置连接。
2.当丙装置中FeC12溶液变黄时,停止加热。
3.打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
4.在乙装置中,打开活塞b,待空气排尽后,将乙中产生的气体通入上述丙装置变黄后的溶液中,一段时间后停止。
5.更新丙中试管,打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
回答下列问题:
(1)甲中发生反应的化学方程式为___________________________________________。
(2)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是__________________。
(3)实验中,证明氧化性Fe3+>SO2的离子方程式为_____________________________。
(4)有I、II、III三组同学分别完成了上述实验,实验结果如下:
上述实验结果一定能够证明氧化性:Cl2>Fe3+>SO2的是___________(用“I”、“II”、“III”代号回答)。
(5)若要用以上甲和丙装置证明氧化性为:Cl2> Fe3+> I2的结论,则步骤为:
①往丙的漏斗中加入两种试剂_________、_________和一种溶剂__________。
②将甲装置中产生的Cl2慢慢通入丙中,观察丙的漏斗中溶液颜色变化。
③如果观察到丙中溶液_______________________________________则结论正确。
④停止通入Cl2。
50 mL1.0 mol·L-1盐酸跟50mL1.1 mol·L-1氢氧化钠溶液在下图装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题。
(1)大小烧杯间填满碎纸条的作用是什么?
(2)大烧杯上如不盖硬纸板,对求得中和热的数值有何影响?
(3)改用60 mL1.0mol·L-1盐酸跟50mL1.1mol·L-1氢氧化钠溶液进行反应,与上述实验相比,所测中和热的数值理论上是否相等(不考虑空气的影响)?简述理由。
(4)用相同浓度和体积的氨水代替NaOH溶液进行实验,为什么测得中和热的数值偏低?
某化学研究性学习小组拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜并测定样品中氧化铜的质量分数,其实验流程如下: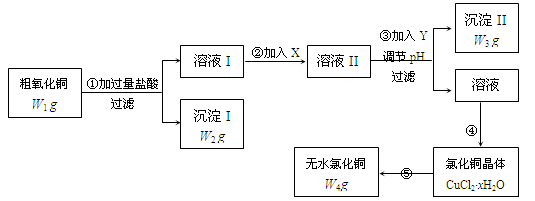
实验过程中的pH调节可参考下表:
| 物质 |
开始沉淀时的pH |
完全沉淀时的pH |
| 氢氧化铁 |
2.7 |
3.7 |
| 氢氧化亚铁 |
7.6 |
9.6 |
| 氢氧化铜 |
5.2 |
6.4 |
回答以下问题:
(1)步骤①过滤操作中所用仪器有铁架台(带铁圈)、漏斗、烧杯等,还需要使用的仪器用品有 。
(2)步骤①中发生的离子反应方程式 。
(3)步骤②溶液I中加入X的目的是 。
(4)试剂Y可选用(填字母),选择的原因是
。
a.氢氧化钠 b.氨水 c.碱式碳酸铜 d.氧化铜
(5)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2·xH2O,其原因是
。
(6) 经检测,CuCl2·xH2O中含水28.6%,则CuCl2·xH2O中x的值为 。