氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| D.以上说法都不正确。 |
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是()
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C.不使电池中渗漏的电解液腐蚀其他物品 |
| D.回收其中的石墨电极 |
镍镉(Ni-Cd)可充电电池可以发生如下反应:
Cd(OH)2+2Ni(OH)2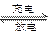 Cd+2NiO(OH)+2H2O。由此可见,该电池的负极材料是()
Cd+2NiO(OH)+2H2O。由此可见,该电池的负极材料是()
| A.Cd | B.NiO(OH) | C.Cd(OH)2 | D.Ni(OH)2 |
将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,即构成甲烷燃料电池,已知通入甲烷的一极,其电极反应为CH4+10OH--8e-====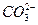 +7H2O;通入氧气的另一极,其电极反应式是2O2+4H2O+8e-====8OH-,下列叙述正确的是()
+7H2O;通入氧气的另一极,其电极反应式是2O2+4H2O+8e-====8OH-,下列叙述正确的是()
| A.通入甲烷的电极为正极 |
| B.正极发生氧化反应 |
| C.该电池使用一段时间后应补充氢氧化钾 |
| D.燃料电池工作时,溶液中的阴离子向正极移动 |
锌溴蓄电池的充、放电的电池总反应为Zn+Br2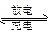 Zn2++2Br-,下列各反应:①Zn-2e-====Zn2+ ②Br2+2e-====2Br- ③2Br--2e-====Br2 ④Zn2++2e-====Zn,其中充电时的阳极和放电时的负极的反应分别是()
Zn2++2Br-,下列各反应:①Zn-2e-====Zn2+ ②Br2+2e-====2Br- ③2Br--2e-====Br2 ④Zn2++2e-====Zn,其中充电时的阳极和放电时的负极的反应分别是()
| A.①② | B.③① | C.④② | D.③② |
pH=a的某电解质溶液中,插入两支惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是( )
| A.NaOH | B.H2SO4 |
| C.AgNO3 | D.Na2SO4 |