(1)将ag氯化钙溶于1.8L水中,恰好使钙离子数与水分子数之比为1:100,则a值为 。
(2)在反应2A+B=3C+2D中,已知3.4gA与3.2gB完全反应,生成4.8gC,又知道D的式量为18,则B的式量是
(3)25.4g 某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是 ;A的相对原子质量是 ;ACl2的化学式是 。
(4) 某混合物由Na2SO4、Al2(SO4)3组成,已知Na、Al两元素的质量之比为23: 9,则Na2SO4和Al2(SO4)3物质的量之比为 ,含1.00mol SO42–的该混合物的质量为 。
下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
| 4 |
⑨ |
(1)在这些元素中,化学性质最不活泼的是:(填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,
(3)写出⑤的最高价氧化物跟⑨的最高价氧化物的水化物在水溶液中反应的离子方程式___________
(4)写出②的最低价氢化物跟它的氧化物的水化物形成的所有化合物的化学式_______
该化合物中含有的化学键有______________
A、B、C、D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
①D在周期表中的位置是____;
②用电子式表示A、B形成化合物的过程:____;
③D2C的电子式为;
如图是几种烷烃分子的球棍模型: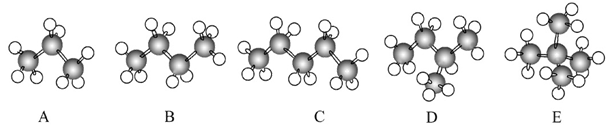
(1)A、B、E三种烷烃的关系为________,C、D、E的关系为_。
(2)用习惯命名法命名:D_______。
(3)E的一氯代物有种,请写出它们的结构简式:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,回答下列问题:
(1)该反的化学反应方程式为;
(2)从开始至2miN,Z的平均反应速率是;
(3)第4分钟时下列叙述正确的是;
| A.该反应已停止 | B.该反应为可逆反应 |
| C.3v(X)=2v(Z) | D.c(X) :c(Y) :c(Z) =" 7" :9 :2 |
某班学生分成甲,乙两小组分别探究硫,氮及其化合物的性质:
(一)甲组同学用下列装置来探究浓硫酸与木炭粉加热反应并验证反应所产生的各种产物。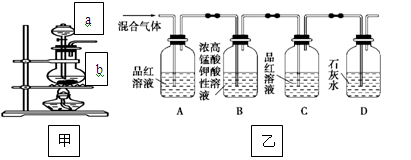
(1)装置甲中盛放浓硫酸的仪器a名称是_______________,
装置甲中仪器b中发生反应的化学方程式为______________________________________
(2)实验中可观察到装置乙中,A瓶的溶液褪色,C瓶的溶液不褪色。
A瓶溶液的作用是__________________________________________________,
B瓶溶液的作用是__________________________________________________,
D瓶溶液的现象是__________________________________________________。
(二)乙组同学用下列装置来证明铜与稀硝酸反应产生一氧化氮,
B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
(1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为________________________________________________________________。
(3)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是。
(4)一段时间后,C中白色沉淀溶解,其原因是________________________。
(5)装置D的作用是_____________________________________________________。