有甲、乙、丙三种溶液,进行如下操作: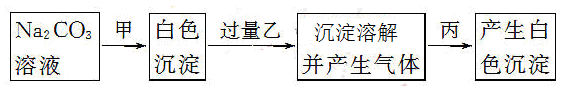
则甲、乙、丙三种溶液可能是
| A.BaCl2、H2SO4、MgCl2 | B.CaCl2、HNO3、BaCl2 |
| C.CaCl2、HNO3、NaCl | D.BaCl2、HCl、Na2SO4 |
短周期主族元素W、R、X、Y、Z,原子序数依次增大。W、X、Y三种元素原子的最外层电子数之和为15,Y原子核电荷数等于W原子核电荷数的2倍,R原子最外层电子数与X原子最外层电子数相差1。下列叙述正确的是
| A.R在化合物中显+1价 | B.最高价氧化物的水化物的碱性:X>R |
| C.原子半径:X>Y>Z | D.简单气态氢化物的热稳定性:Y>W |
温度不变恒容的容器中0.1mol·L-1H2进行反应H2 2H,若某段时间内H2浓度由0.06mol·L-1降到0.036mol·L-1所需的反应时间为12s ,则反应起始时H2浓度由0.1mol·L-1降到0.06mol·L-1需的时间为
2H,若某段时间内H2浓度由0.06mol·L-1降到0.036mol·L-1所需的反应时间为12s ,则反应起始时H2浓度由0.1mol·L-1降到0.06mol·L-1需的时间为
| A.等于24s | B.等于20s | C.大于20s | D.小于20s |
有A、B、C、D、E五种金属元素.在相同条件下,B元素的最高价氧化物对应水化物的碱性比A的弱;A、B单质均可以从C盐溶液中置换出C;D单质可以与冷水剧烈反应并放出氢气;A、B、C、E四种单质分别投入盐酸中,只有E不放出氢气.则五种金属元素的金属性由强到弱的顺序为
A.D>B>A>C>E B.D>A>B>C>E
C.A>B>C>E>D D.D>E>B>A>C
在下列有关晶体的叙述中错误的是
| A.稀有气体的原子能形成分子晶体 | B.离子晶体中,一定存在离子键 |
| C.原子晶体中,只存在共价键 | D.金属晶体的熔沸点均很高 |
CO2气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO2气体,这两个变化过程中需要克服的作用分别是
| A.分子间作用力,离子键 | B.化学键,分子间作用力 |
| C.化学键,化学键 | D.分子间作用力,分子间作用力 |