W、X、y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为________________________________________________________________ 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为________。将等体积、等浓度的W
的最高价氧化物对应的水化物和Y的氢化物混合,其化学方程式为__________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_____________________________________________________。
(4)W、X、Y、Z四种元素简单离子的离子半径由小到大的顺序是_______________。
(4分)某简单微粒的结构示意图为:
(1)当y=1时,若该微粒成电中性,则x=________
(2)当y=8时,若该微粒带有2个单位负电荷,则该微粒的符号为_______
(1)4.5g水与________g硫酸所含的分子数相等,它们所含氧原子数之比是 。
。
(2)某金属氧化物的化学式为M2O3,电子总数为76,已知氧原子核内有8个中子,M2O3的相对分子质量为160,则M原子核内中子数是。
(3)某些化学试剂可用于净水。水处理中使用的一种无机高分子混凝剂的化学式可表示为[Al2(OH)nClm·YH2O]x,式中m等于。
| A.3-n | B.6-n | C.6+n | D.3+n |
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,W的单质为淡黄色固体,Y、Z左右相邻,Z、W位于同主族。
⑴ X元素是;W的原子结构示意图。
⑵ X与W组成的化合物中存在键(填“离子”“共价”)。
⑶ Y、Z形成的简单离子的半径由大到小的顺序为。
⑷工业上由X的单质与Y的单质化合生成1molA气体时放出46.2kJ的热量,写出该反应的热化学方程式。
⑸由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a. 取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时 间白色沉淀变为灰绿色,最终变为红褐色;
间白色沉淀变为灰绿色,最终变为红褐色;
b. 另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为。
② 已知1 mol·L—1 100mL B的溶液能与1 mol·L—1 20mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式。
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为。在X极附近观察到的实验现象是。
②Y电极上的电极反应式为。
③若阴极生成气体22.4L(标况下) 电路中转移电子mol
(2)如要用电解方法精炼粗铜,
①电解液a选用溶液,则
②X电极反应式为,
③Y电极的材料是。
工业上需要利用一批回收的含铜废料制造胆矾(CuSO4·5H2O)。该废料中各种成份含量如下:Cu和CuO约占87%,其它为Al、Fe、Si及其氧化物,还有少量的难溶物质。工艺流程为: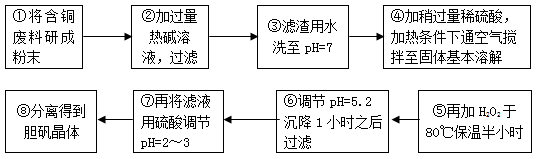
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Cu(OH)2 |
Mg(OH)2 |
Fe(OH)2 |
| pH |
5.2 |
3.1 |
6.7 |
9.4 |
9.7 |
回答:
(1)步骤①中为什么要将含铜废料研磨成粉状? 。
。
(2)步骤⑤中H2O2参加反应的离子方程式: 。
。
(3)步骤⑥中调节溶液pH时适宜的物质是。(填序号);
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Cu(OH)2 E.MgCO3
步骤⑥中滤渣成份的化学式。
(4)步骤⑦中用硫酸调节pH=2~3的原因是。
(5)步骤⑧的分离操作是: , 冷却结晶,。