下列实验操作中,正确的是( )
| A.利用丁达尔效应可以区分溶液和胶体 |
| B.用滤纸过滤可以除去溶液中的胶体粒子 |
| C.向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体 |
| D.向Fe(OH)3胶体加入足量稀盐酸后,依然有丁达尔现象 |
下列说法中,正确的是
| A.酸性:盐酸>氢硫酸(H2S),故非金属性:Cl>S |
| B.第二周期元素的最高正化合价从左到右依次升高 |
| C.共价化合物中只存在共价键离子化合物中一定含有离子键 |
| D.元素原子的最外层电子数越多,得电子能力越强,失电子能力越弱 |
已知,I2(aq)+I-(aq) I3-(aq)。某I2、、KI混合溶液中,c(I3-)与温度(T)的关系如下图所示(曲线上任何一点都表示平衡状态)。下列说法中,正确的是
I3-(aq)。某I2、、KI混合溶液中,c(I3-)与温度(T)的关系如下图所示(曲线上任何一点都表示平衡状态)。下列说法中,正确的是
A.反应 I2(aq)+I-(aq)  I3-(aq)的△H>0 I3-(aq)的△H>0 |
| B.状态A的c(I2)比状态D的小 |
| C.A点对应的反应速率大于C点对应的反应速率 |
| D.其他条件不变,向溶液中加入KI固体,平衡由C点移动到D点 |
下列有关平衡常数的说法中,正确的是()
| A.改变条件,反应物的转化率增大,平衡常数也一定增大 |
B.反应2NO2(g)  N2O4(g) △H<0,升高温度该反应平衡常数增大 N2O4(g) △H<0,升高温度该反应平衡常数增大 |
| C.对于给定可逆反应,温度一定时,其正、逆反应的平衡常数相等 |
D.平衡常数为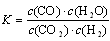 的反应,化学方程式为CO2+H2 的反应,化学方程式为CO2+H2 CO+H2O CO+H2O |
在t℃时,将a g NH3完全溶于水,得到V mL溶液,设该溶液的密度为ρg·cm-3,质量分数为ω,其中含NH4+的物质的量为b mol。下列叙述中不正确的是
A.溶质的质量分数为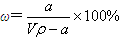 |
B.溶质的物质的量浓度 |
C.溶液中c(OH-)=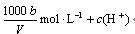 |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数小于0.5ω |
已知:2FeCl3+2KI===2FeCl2+2KCl+I2;2FeCl2+Cl2==2FeCl3。下列微粒还原性由强到弱的顺序中,正确的是
| A.Fe2+>Cl->I- | B.I->Fe2+>Cl- | C.Cl->Fe2+>I- | D.I->Cl->Fe2+ |