实验室常利用甲醛(HCHO)法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4+ +6HCHO =3H++6H2O+(CH2)6N4H+ [滴定时,1 mol (CH2)6N4H+与 l mol H+相当,然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500 g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤III填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积_______(填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察____________。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时现象:__________________________________________________。
(2)滴定结果如下表所示:
| 滴定 次数 |
待测溶液的体积 /mL |
标准溶液的体积/mL |
|
| 滴定前刻度 |
滴定后刻度 |
||
| 1 |
25.00 |
1.02 |
21.03 |
| 2 |
25.00 |
2.00 |
21.99 |
| 3 |
25.00 |
0.20 |
20.20 |
若NaOH标准溶液的浓度为0.1010 mol·L-1,则该样品中氮的质量分数为___________。
某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是 。
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(划斜线部分不必填写):
| 序号 |
实验内容 |
实验现象 |
离子方程式 |
实验结论 |
| ① |
在FeCl2溶液中滴入适量氯水 |
溶液由浅绿色变为棕黄色 |
Fe2+具有还原性 |
|
| ② |
在FeCl2溶液中加入锌片 |
 |
Zn+Fe2+=Zn2++Fe |
|
| ③ |
在FeCl3溶液中加入足量铁粉 |
Fe+2Fe3+=3 Fe2+ |
Fe3+具有氧化性 |
|
| ④ |
 |
Fe3+具有氧化性 |
实验结论:。
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:。(填序号)
A、Cl2
B、Na
C、Na+
D、Cl-
E、SO2
F、盐酸
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液。那么保存亚铁盐溶液时应该如何防止亚铁盐被氧化。
26.(10分)孔雀石的主要成分是CuCO3·Cu(OH)2,还含有少量的SiO2和铁的化合物。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下: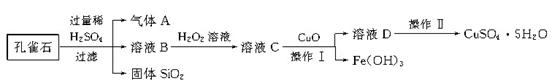
请回答下列问题:
(1)溶液B中的金属离子有Cu2+、Fe2+、Fe3+。若要检验溶液B中Fe2+,最适宜选用的试剂为________(填字母)。
a.KMnO4溶液 b.铁粉c.NaCl溶液 d.KSCN溶液
(2)向溶液B中加入H2O2溶液的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:____________________________;实验室选用H2O2而不用Cl2作氧化剂,除考虑环保因素外,另一原因是________________________。
(3)由溶液D获得CuSO4·5H2O,需要经过加热蒸发,________,过滤等操作。除烧杯、漏斗外,过滤操作还用到了另一玻璃仪器,该仪器在此操作中的主要作用是____。
(4)将制得的胆矾样品用热重仪进行热重分析,热重仪原理及热重计录如下:
写出212~250 ℃温度范围内发生反应的化学方程式:________________________。
葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
CH2OH(CHOH)4CHO+Br2+H2O → C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3 → Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 |
葡萄糖酸钙 |
葡萄糖酸 |
溴化钙 |
氯化钙 |
| 水中的溶解性 |
可溶于冷水易溶于热水 |
可溶 |
易溶 |
易溶 |
| 乙醇中的溶解性 |
微溶 |
微溶 |
可溶 |
可溶 |
实验流程如下:
请回答下列问题:
(1)第 ① 步中溴水氧化葡萄糖时,下列装置最合适的是_________(填序号)。 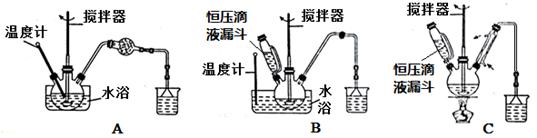
(2)第 ② 步充分反应后CaCO3固体需有剩余,其目的是_______________________。
(3)本实验中不宜用CaCl2替代CaCO3,理由是_______________________________。
(4)第 ③ 步需趁热过滤,其原因是_________________________________________。
(5)葡萄糖溶液与新制Cu(OH)2悬浊液反应的化学方程式为。
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下
(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入________(填“A”或“B”),再滴加另一反应物.
(2)如图所示,过滤操作中的一处错误是________________________.
(3)判断流程中沉淀是否洗净所采取的方法是____________________________________________.
(4)高温焙烧时,用于盛放固体的仪器名称是________________.
(5)无水AlCl3(183°C升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备:
装置 B中盛放饱和NaCl溶液,该装置的主要作用是___________________.F中试剂的作用是_____________________.用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为_________________________.
间硝基苯胺(Mr=128)是一种重要的染料中间体。它是一种黄色针状结晶,微溶于水,随温度升高溶解度增大,溶于乙醇、乙醚、甲醇。间硝基苯胺可选用间二硝基苯与碱金属多硫化物进行选择性还原,其反应式如下: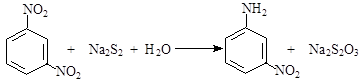
已知:R-NH2 + H+ → R-NH3+
实验步骤:
①在100mL锥形瓶中加入8g结晶硫化钠与30mL水,搅拌溶解。再加入2g硫黄粉,缓缓加热并不断搅拌到硫黄粉全部溶解,冷却后备用。
②在150mL三颈烧瓶中加入4.74g间二硝基苯(Mr=158)与40mL水,安装机械搅拌装置、滴液漏斗和回流冷凝管如图所示,将步骤①配制的多硫化钠溶液加入滴液漏斗。
③加热三颈烧瓶至瓶内微微沸腾,开动搅拌使间二硝基苯与水形成悬浮液。慢慢滴加多硫化钠溶液,滴加完毕后继续搅拌回流30min。移去热源,用冷水浴使反应物迅速冷却到室温后,减压过滤,滤饼洗涤三次。
④在150mL某容器中配制稀盐酸(30mL水加7mL浓盐酸),将上述粗产物转移进该容器,加热并用玻璃棒搅拌,使间硝基苯胺溶解,冷却到室温后减压过滤。
⑤冷却滤液,在搅拌下滴加过量浓氨水到pH=8,滤液中逐渐析出黄色的间硝基苯胺。
⑥冷却到室温后减压过滤,洗涤滤饼到中性,抽干,产物重结晶提纯,在红外灯下干燥,称重,得2.56g。
回答下列问题:
(1)滴液漏斗较普通分液漏斗的优点;第④步中配制稀盐酸的容器名称为。
(2)间二硝基苯和间硝基苯胺都有毒,因此该实验应在内进行。
(3)在铁和盐酸作用制得初生态氢原子(还原性远强于碱金属多硫化物)也可以将硝基还原为氨基,却未被采用,其可能原因为。
(4)第④步用盐酸溶解粗产品,而不用水的原因。
(5)第③步中滤饼洗涤三次,可选用的洗涤剂为( );第⑥步产物要进行重结晶,可选用的试剂为( )。
| A.冷水 | B.热水 | C.乙醚 | D.乙醇 |
(6)第③步中,搅拌使间二硝基苯与水形成悬浮液后再滴加多硫化钠溶液,其原因为。
(7)第⑥步中要将滤饼洗涤到中性,检验方法为。
(8)该反应的产率为。