某化学兴趣小组用下图装置电解CuSO4溶液,测定铜的相对分子质量。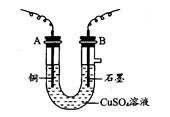
(1)若实验中测定在标准状况下放出的氧气的体积VL,A连接直流电源的__________ (填“正极”或“负极”)。
(2)电解开始一段时间后,在U形管中可观察到的现象-____________________________。
电解的离子方程式为 。
(3)实验中还需测定的数据是_______________(填写序号)。
①A极的质量增重m g ②B极的质量增重m g
(4)下列实验操作中必要的是____________(填字母)。
| A.称量电解前电极的质量 |
| B.电解后,电极在烘干称重前,必须用蒸馏水冲洗 |
| C.刮下电解过程中电极上析出的铜,并清洗、称重 |
| D.电极在烘干称重的操作中必须按“烘干—称重一再烘干一再称重”进行 |
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为:_______________________(用含有m、V的计算式表示)。
(6)如果用碱性(KOH为电解质)甲醇燃料电池作为电源进行实验,放电时负极的电极反应式为 。
化学学科中的平衡理论主要包括:化学平衡、电离平衡和水解平衡三种,且均符合勒夏特列原理。请回答下列问题:
Ⅰ、在恒容密闭容器中,发生反应3A(g)+B(g) 2C(g) ΔH=Q kJ/mol。回答下列问题:
2C(g) ΔH=Q kJ/mol。回答下列问题:
(1)写出该反应平衡常数的表达式__________。
(2)下列各项能作为判断该反应达到化学平衡状态的依据是________(填序号)。
① v(A)=3v(B)②混合气体的密度保持不变
③有3 mol A消耗的同时有1 mol B生成 ④C的浓度保持不变
(3)根据实验测得的数据可知,温度越高该反应的化学平衡常数越大,则Q______0(填“大于”或“小于”)。
Ⅱ、(1)室温下,取pH=2的盐酸和醋酸溶液各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是________(填 “a”或“b”)。设盐酸中加入Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1________m2(选填“<”、“=”或“>”)。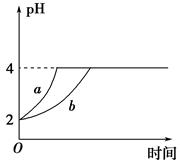
(2)若室温下pH=2的盐酸和醋酸溶液各 100 mL,分别加水稀释后使pH=4,设盐酸中加入水的体积为V1,醋酸溶液中加入的水的体积为V2,则 V1______V2(填“<”“=”或“>”)。
Ⅲ、常温下,浓度均为0.1 mol/L 的下列六种溶液的pH如下表:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
(1)上述盐溶液中的阴离子,结合H+能力最强的是
(2)根据表中数据判断,浓度均为0.01 mol/L 的下列五种物质的溶液中,酸性最强的是_______ (填编号) ; 将各溶液分别稀释100倍, pH变化最小的是(填编号) 。
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
(3)据上表数据,请你判断下列反应不能成立的是 (填编号)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2C6H5 ONa=Na2CO3+2C6H5OH
Ⅳ、已知:ZnCl2·xH2O易溶于水,且其浓的水溶液呈较强酸性;SOCl2 (氯化亚砜)极易和水发生如下反应:SOCl2+H2O=SO2+2HCl。实验室中制取无水氯化锌采用ZnCl2·xH2O与SOCl2混合加热的方法。试回答:
SOCl2的作用是___________________________________。
醋酸是重要的一元酸,在有机和无机反应中都有应用.现有25℃时pH=3的醋酸。请回答下列问题:
(1)若向醋酸中加入少量醋酸钠固体,此时溶液中c(H+)/c(CH3COOH)将
(填“增大”、“减小”或“不变”)。
(2) 若向醋酸中加入稀NaOH溶液,使其恰好完全反应,所得溶液的pH 7
(填“>”、“<”或“=”);用离子方程式表示其原因 。
(3)若向醋酸中加入稀NaOH溶液至溶液恰好呈中性,此时c(Na+)c(CH3COO-)(填“>”“<”“=”)。
(1)①常温下,pH=3的盐酸和pH=11的氢氧化钡等 体积混合,溶液的pH=。
②常温下pH=3的盐酸和pH=6的盐酸等体积混合,溶液的pH=。(lg2=0.3)
(2)在某温度下,H2O的离子积常数为1×10-13,则该温度下
①某溶液中的H+浓度为1×10-7mol/L,则该溶液呈性。
②0.01mol/LNaOH溶液的pH=。
③99mL pH=1的H2SO4溶液与101mL pH=12的KOH溶液混合后,溶液的pH=。
反应2A B+C,在某一温度时,达到平衡。
B+C,在某一温度时,达到平衡。
(1)若温度升高,化学平衡正向移动,则正反应是_____热反应;
(2)若B是 固体,降低压强时,平衡逆向移动,则A是_____态;
(3)若A是气态,加压时,平衡不移 动,则B为_______态,C为______态。
今有化合物:
(1)请写出丙中含氧官能团的名称:。
(2)请判别上述哪些化合物互为同分异构体:。
(3)请分别写出鉴别甲、乙、丙化合物的方法。(指明所选 试剂及主要现象即可)
鉴别甲的方法:
鉴别乙的方法:
鉴别丙的方法:
(4)请按酸性由强至弱排列甲、乙、丙的顺序:。