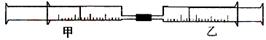
如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定)。
| 实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
| 1 |
40 mL HCl |
40 mLNH3 |
产生白烟 |
| 2 |
40 mL Cl2 |
10mL 水 |
剩余气体为20mL |
| 3 |
30 mL NO |
15 mL O2 |
|
| 4 |
20 mL AlCl3溶液 |
10 mL NaOH溶液 |
生成白色沉淀,后消失 |
(1)如果实验1甲针筒内改装30 mL Cl2 ,乙针筒内仍为40 mLNH3,实验时,甲针筒内也有白烟产生。写出有关反应的化学方程式 。
(2)由实验2可知,常温常压下氯气在水中的溶解度为 。
(3)实验3 反应后甲针筒内气体的体积为 。
(4)实验4中,AlCl3溶液浓度为0.1mol/L,如果最后白色沉淀全部消失,则NaOH溶液浓度至少为 mol/L。
(5)将上述装置做以下改进:在甲、乙针筒之间连接一段硬质玻璃管,如下图。在A处装一种浅黄色的粉末,乙针筒内是一种常见的气体,甲针筒无气体。将乙针筒内气体压入甲针筒内,发现气体体积是原来的一半。A处的物质是 ,甲针筒内的气体为 。

(6)有学生用上述改进后的装置测定空气中氧气的体积分数(加热用酒精灯未画出)。乙针筒内装有50 mL空气。实验时,用酒精灯对A处物质进行加热,经反复慢慢推拉两针筒的活塞,反应完毕,恢复至室温,测得剩余气体为40.5mL。
①A处的物质是 (选填编号)。
a.碳粉 b.二氧化锰 c.铜粉 d.氧化铜
②已知空气中氧气的体积分数为0.2,则该实验的相对误差为 。
根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
(1)废水I若采用CO2处理,离子方程式是。
(2)废水II常用明矾处理。实验中发现废水中的c(HCO-3)越大,净水效果越好,这是因为。
(3)废水III中的汞元素存在如下转化 (在空格上填相应的化学式):
(在空格上填相应的化学式):
Hg2+ =====CH3Hg++H+
我国规定,Hg2+的排放标准不能超过0.05mg/L。某工厂排放的1m3废水中含Hg2+ 3×10-4mol,是否达到了排放标准(填“是”或“否”)。
(4)废水IV常用Cl2将CN-氧化成两种无毒气体,则该反应的离子方程式为
.
海洋约占地球表面积的71%,海水化学资源的利用具有非常广阔的前景。
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、、可制得精盐。
(2)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如下: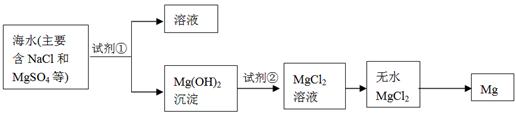
①为了使MgSO4转化为Mg(OH) 2,试剂①可以选用,要使MgSO4完全转化为沉淀,加入试剂①的量应;
②试剂②可以选用;
③试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是。
A. |
B. |
C.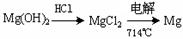 |
D.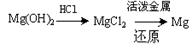 |
(3)溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下: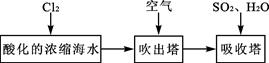
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
①A装置中通入a气体的目的是(用离子方程式表示);
②A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是
;
③反应过程中,B装置中有SO42-生成。检验SO42-的方法是;
④C装置的作用是。
有机化学知识在生活中应用广泛 。
。
(1)糖类、油脂和蛋白质是动物性和植物性食物中的基本营养物质。
①下列有关说法中,正确的是;
A.棉、麻、木材、蚕丝的主要成分都是纤维素
B.油脂是产生能量最高的营养物质
C.蛋白质在人体内发生水解最终生成氨基酸
D.糖类都是有甜味的物质
E.淀粉、纤维素、蛋白质都是天然高分子化合物
F.硫酸铵或乙酸铅溶液加入到蛋白质溶液中,蛋白质都能从溶液中析出
②葡萄糖是最重要、最简单的单糖,除了是一种营养物质,还能用在制镜等工业上。写出
葡萄糖发生银镜反应的化学方程式:。
(2)苹果酸常用作汽水、糖果的添加剂,其结构简式为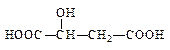 ,该分子中官能团的名称为,可以和醇类物质发生反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为。
,该分子中官能团的名称为,可以和醇类物质发生反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为。
(3)实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)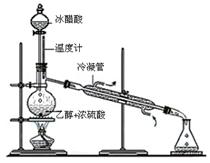
①在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是;
②生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的有(填序号);
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的浓度不再变化
③现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程 图。
图。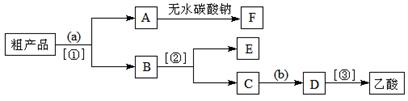
试剂a是,分离方法①是;分离方法②是,试剂b 是;
是;
④写出C → D 反应的化学方程式。
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl =" NaCl" + H2O,
B.2FeCl3 + Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A.B.。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是(填“锌”或“铜”),发生反应(填“氧化”或“还原”);
②正极的电极反应式为;
③产生这些气体共需转移电子mol。
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| A |
有三个电子层,K、M层电子数之和等于L层电子数 |
| B |
短周期中金属性最强 |
| C |
常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D |
元素最高正价是+7价 |
(1)用化学用语回答下列问题:
①A元素在周期表中的位置;
②B元素原子结构示意图;
③C单质分子的电子式;用电子式表示A和B元素组成的化合物的形成过程;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素。
(2)元 素D与元素A相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是(填选项序号)。
素D与元素A相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是(填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是(写化学式)。
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去)。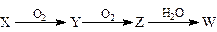
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:;生成该白色沉淀的化学方程式为;
② 若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:。
若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:。