由C、Cu、FeCO3、铜锈[主要成分为Cu2(OH)2CO3]组成的固体混合物,进行了如下所示的实验过程:
回答下列问题:
(1)无色气体1的成分是: 。
(2)混合物乙中加入NaNO3后,写出一个可能产生无色气体2的反应的离子方程式:
(3)溶液X中含有的金属阳离子是 。
(4)无色气体3成分是 ,已知固体混合物丁的的质量为5.6g,在标准状况下无色气体3的体积为14.56L,求无色气体3各成分的物质的量: 。(写出具体的计算过程)
1)49 g硫酸的物质的量为mol,若在水中完全电离可产生 molH+ , ______mol
molH+ , ______mol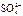 .若有一定量的硫酸完全电离产生
.若有一定量的硫酸完全电离产生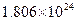 个
个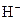 ,此硫酸的质量为 _______g.
,此硫酸的质量为 _______g.
(2)标准状况下,11.2L的H2S气体质量为17g,则H2S的摩尔质量是,相对分子质量为; 等物质的量的NH3与H2S质量比为; 1.7g氨气与mol H2O含有的电子数相等。
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如下图所示,则上述CO2转化为甲醇的反应的ΔH3
0(填“>”、“<”或“=”)。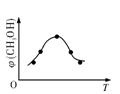
②在一恒温恒容密闭容器中充入1mol CO2和3mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。下列说法正确的是 (填字母代号)。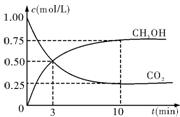
| A.第10min后,向该容器中再充入1mol CO2和3mol H2,则再次达到平衡时c(CH3OH)=1.5mol·L-1 |
B.0~10min内,氢气的平均反应 速率为0.075mol/(L·min) 速率为0.075mol/(L·min) |
| C.达到平衡时,氢气的转化率为0.75 |
| D.该温度下,反应的平衡常数的值为3/16 |
E.升高温度将使n(CH3OH)/n(CO2)减小
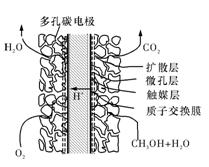
③甲醇燃料电池结构如下图所示。其工作时正极的电极反应式可表示为
。
(3)脱硫。某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥。设烟气中的SO2、NO2的物质的量之比为1∶1,则该反应的化学方程式为 。
(4)硫 酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为: NH+H2O
酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为: NH+H2O NH3·H2O+H+ ;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中:c(Na+)+c(H+) c(NO)+c(OH-)(填写“>”“=”或“<”)。
NH3·H2O+H+ ;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中:c(Na+)+c(H+) c(NO)+c(OH-)(填写“>”“=”或“<”)。
A、B、C三种强电解质,它们在水中电离出的离子为Na+、Ag+、NO、SO、Cl-,在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了10.8克。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题: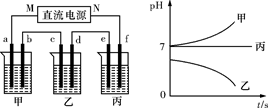
(1)M为电源的 极(填写“正”或“负”),甲、乙两个烧杯中的电解质分别为 、 (填写化学式)。
(2)计算电极f上生成的气体为 mol。
(3)写出乙烧杯中的电解反应方程式: 。
(4)若电解后甲溶液的体积为10L,则该溶液的pH为 。
(5)要使丙恢复到原来的状态,应加入适量的 (填 写化学式)。
写化学式)。
利用芳香烃X和链烃Y可以合成紫外线吸收剂BAD,已知G不能发生银镜反应,BAD结构简式为:
OHCOOCCH3CH3OOCOH
BAD的合成路线如下: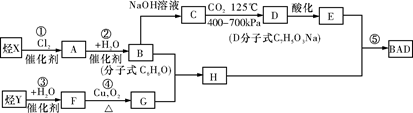
试回答下列问题:
(1)写出下列物质的结构简式:Y ;D;
H 。
(2)属于取代反应的有 ①②⑤ (填数字序号)。
(3)1mol BAD最多可与含 mol NaOH的溶液完全反应。
(4)写出反应④的化学方程式 。
A、B、C、D四种短周期元素的原子半径依次减小,在周期表中B与A、C相邻,C的最外层电子数 是其电子总数的3/4,D能分别与A、B、C形成电子总数相等的化合物X、Y、Z。试回答:
是其电子总数的3/4,D能分别与A、B、C形成电子总数相等的化合物X、Y、Z。试回答:
(1)在X、Y、Z三种化合物中稳定性由强到弱的顺序是 。
(2)若由A、B、C、D四种元素组成一种离子化合物,1mol该化合物中 含有10mol原子,则该化合物受热分解的化学方程式为 。
含有10mol原子,则该化合物受热分解的化学方程式为 。
(3)Y跟HCl反应生成固体W。该固体跟有毒的工业盐NaNO2的水溶液混合加热,NaNO2中的化学键被完全破坏,当有1mol NaNO2发生反应时,共有3mol电子转移,该反应的化学方程式为 。
(4)常温下,pH=5的W的水溶液和HCl的稀 溶液中由水电离出来的H+离子浓度之比为 。
溶液中由水电离出来的H+离子浓度之比为 。