暖宝宝是一种防寒用品,如图所示。暖宝宝中的主要成分有哪些?发热的原因是什么?
(1)小明探究:暖宝宝中的主要成分是什么?
剪开内包装袋,倒出其中的粉末,发现呈黑色。
【提出猜想】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化三铁中的一种或几种。
【初步验证】将磁铁靠近黑色粉末,部分被吸引。
【查阅资料】四氧化三铁具有磁性,能被磁铁吸引;炭粉、二氧化锰不与稀硫酸反应;氧化铜与稀硫酸反应后溶液呈蓝色。
【得出结论】该黑色粉末可能含有(写物质的名称) 。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
取黑色粉末加足量稀硫酸 |
固体部分溶解,有气泡产生,溶液无蓝色 |
| ② |
取实验①的残渣灼烧,将内壁涂 有澄清石灰水的小烧杯罩在上方 |
澄清石灰水变浑浊 |
由实验①可知,该黑色粉末中肯定含_____________,肯定不含______________。
由实验②可知,该黑色粉末肯定含 。
(2)小明思考:暖宝宝为什么会发热?
【查阅资料】暖宝宝中的铁粉在空气中发生了缓慢氧化,进而放出热量。由此可见,
人们可以利用化学反应放出的能量,请再举一例:___________________。
(3)人们利用化学反应还可以_______________________。
(4)课外小组的同学研究的课题是测定贝壳中碳酸钙的质量分数,他们取25g贝壳粉碎后放入烧杯中,向杯中倒入稀盐酸,当倒入100g稀盐酸后发现不再产生气泡,并测得烧杯内固体和液体总质量为120.6g (杂质不反应)。求贝壳中碳酸钙的质量分数。
近几年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化
学方程式为:5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2 X ”。这个化学方程式中
最后一种物质X的化学式是:。
(2)“二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊。”请写出二氧化硫与澄清石灰水反应的化学方程式:。并写出实验室制取二氧化碳的化学方程式:。
根据上述资料,甲同学、乙同学和丙同学分别设计实验方案进行探究。
【实验探究】(3)甲同学:“实验操作”:甲同学进行了如下图所示A、B两步实验: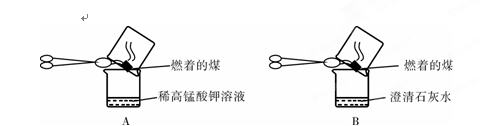
“实验现象”: A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(4)乙同学认为甲同学的实验方案不合理,其理由是:。
(5)丙同学:
“实验操作”:丙同学进行了如下图所示实验(部分装置在图中略去):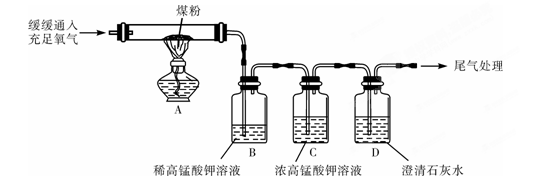
【探究与结论】(6)上图C装置的作用是。
(7)要证明煤中含有碳元素和硫元素的现象是:丙同学的实验中。
为验证混合气体由H2、CO和HC1组成,请从下图中选用适当的实验装置设
计一个实验,并回答下列问题
(1)连接选用装置的正确顺序是(只要求写出图中装置的序号)
(2)所用装置的连接顺序是(填各接口的字母,连接胶省略,装置之间用“→”连接)混合气体→。
(3)首先选用的装置的作用,第二步选用的装置的作用。
(4)简述尾气处理方法。
明矾[化学式为KAl(SO4)2·12H2O]是一种常用的净水剂。小华同学为了探究明矾的净水原理,进行了如下实验探究:
【提出问题】明矾为什么能够净水?
【查阅资料】材料一:净水原理是,净水剂具有较大表面积或者净水剂粒子与水反应生成表面积较大的物质,把水中的细小漂浮颗粒吸附到表面,使其密度加大并下沉。
材料二:明矾[KAl(SO4)2·12H2O]在水溶液中可以解离出K+、Al3+、SO42-。
【提出猜想】猜想1:K+能与水反应产生表面积较大的物质。
猜想2:Al3+能与水反应产生表面积较大的物质。
猜想3:SO42-能与水反应产生表面积较大的物质。
猜想4:K+、Al3+、SO42-均能与水反应产生表面积较大的物质。
【完成实验】
| 实验 序号 |
水样(稍浑浊) 体积(mL) |
实验操作 |
观测 时间 |
实验现象 |
| ① |
20 |
向水样中加入KCl溶液 |
5分钟 |
仍浑浊 |
| ② |
20 |
向水样中加入Na2SO4溶液 |
5分钟 |
仍浑浊 |
| ③ |
20 |
向水样中加入Al2(SO4)3溶液 |
5分钟 |
变澄清 |
| ④ |
20 |
向水样中加入AlCl3溶液 |
5分钟 |
变澄清 |
【得出结论】实验证明SO42-无净水作用,实验证明K+无净水作用;
猜想成立。
【交流反思】(1)小芳同学认为实验①和④是多余的,你(填“支持”或“不支持”)她的观点,理由是。
(2)(填“能”或“不能”)把实验③省去。
(3)小莉同学联想到自来水的生产过程中会用到活性炭去除水中异味,他认为活性炭的作用原理与明矾相同,你同意她的观点吗?[注意:若答对本小题奖励4分,化学试卷总分不超过60分。]
(填“同意”或“不同意”),理由是。
随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重。醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用。交警对呼气酒精检验的原理是:橙色的K2Cr2O7酸性溶液遇乙醇会迅速变成蓝绿色。
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸。小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性。在加热条件下,可以把氧化铜还原为单质铜。
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性。
【提出猜想】猜想1:只有乙醇
猜想2:只有乙酸
猜想3:
【实验探究】
| 实验操作 |
实验现象 |
实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 |
猜想1成立 |
|
| ② |
【实验反思】操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?,理由是。
某化肥厂生产合成氨(NH3)的原料是煤、空气、水,生产简要流程如下(合成塔中需高温、高压),请回答下列问题:
(1)碳化塔的作用是,液氨储槽中发生的是(填“物理”或“化学”)变化。
(2)煤气发生炉中的主要反应为:①C+O2 =CO2;②C+H2O=CO+H2。两个反应必须进行调控,才能保持所需要达到的炉内温度,据此判断:反应②(填“放出”或“吸收”)热量,反应①的主要作用是。
(3)若煤气发生炉排出的混合气体中氧气残留过多,则(填“需要”或“不需要”)除去,理由是。