下列物质:①清新的空气;②甲烷;③过氧化氢溶液;④水银;⑤冰水共存物;⑥加热高锰酸钾完全分解后的固体剩余物;⑦液氧;⑧矿泉水。其中属于混合物的有(序号)________________;属于单质的有(化学式)_____________;属于化合物的有(化学式)_________________。
以化合价位纵坐标,物质的类别为横坐标所绘制的图象叫价类图、如图为硫的价类图,请分析该图后填空: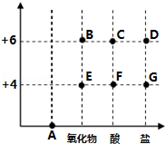
(1)E点表示的是二氧化硫,写出它的一条物理性质 ;
(2)如图中可表示K2SO4,这种盐的点是 (填字母);
(3)A点表示的物质类别是 ;
(4)写出由B点表示的化合物与氢氧化钠溶液反应的化学方程式
如图A是某金属元素形成微粒的结构示意图:该金属在空气中燃烧时放出大量的热并发出耀眼的白光,图B是该反应的微观示意图、请根据以上信息回答下列问题: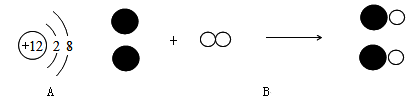
(1)该金属元素原子核外电子数= ,图A所示微粒的符号为 ;写出一种与图A所示具有相同电子层结构的阴离子的符号
(2)图B所示的化学方程式:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: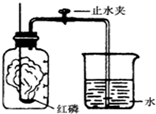
①将图中的集气瓶分为5等份,并作好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷需稍过量,目的是___________;
(2)步骤②集气瓶中的现象是_____________,步骤③中打开止水夹后观察到的现象是_____,由此可得出空气中氧气的体积分数约为_______
(3)该实验还可推论出氮气_______(填“易”或“难”)溶于水和其化学性质______(填“活泼”或“不活泼”)的结论.
实验室制取气体时所需的一些装置如图所示,请回答下列问题: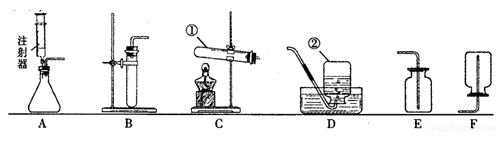
(1)写出指定仪器的名称:① ; ② ;
(2)小明同学选择C装置用氯酸钾和二氧化锰制取一瓶干燥的氧气,他应选择的收集装置是 (填字母);在该反应中MnO2可以重复使用,理由是 .
(3)小华同学想用高锰酸钾为原料来制取一瓶较纯净氧气,应选择的发生装置是 (填字母),收集装置是 .反应的文字表达式是 ,属于 (填基本反应类型)。
(4)实验室在常温下用块状电石与水反应制取不易溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是 (填字母)。
以下是小瑛和小方设计的证明分子运动的实验:小方的实验如图(1)所示,图(2)是小瑛的实验,在锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.
(1)小瑛观察到的现象是___________ 小方观察到的现象是________他可以得到的结论是_____________
(2)小方在大烧杯外放一杯酚酞溶液的目是_____________
(3)请你就两位学生的操作过程、药品用量、以及实验的严密性或其它方面作出比较性的评价_____