二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。ClO2是一种黄绿色的气体,易溶于水。实验室以NH4C1、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下: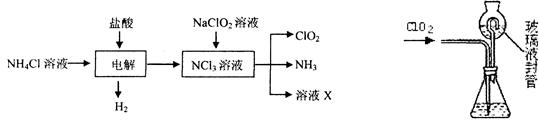
⑴ 写出电解时发生反应的化学方式: 。
⑵ 测定ClO2(如右图)的过程如下:在锥形瓶中加入足最的碘化钾,用100 mL水溶解后,再加3 mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去V mL硫代硫酸钠溶液。
① ClO2通入锥形瓶与酸性碘化钾溶液反应,反应的离子方程式为: 。
② 装置中玻璃液封管的作用是 、 。
③ 滴定至终点的现象是 。
④ 测得ClO2的质量m(ClO2)= 。(用含c、V的代数式表示)
请回答下列问题。
苯佐卡因是一种医用麻醉药品,学名对氨基苯甲酸乙酯。用芳香烃A为原料合成苯佐卡因E的路线如下:
请回答:
⑴写出结构简式 B ▲C ▲。
⑵写出反应类型①▲② ▲。
⑶化合物D经聚合反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域。写出该聚合反应的化学方程式:
▲。
⑷下列化合物中能与E发生化学反应的是▲。
a. HCl b. NaCl c. Na2CO3 d. NaOH
⑸除 、
、 、
、 外,符合下列条件的化合物E的同分异构体有▲种。
外,符合下列条件的化合物E的同分异构体有▲种。
i. 为1,4—二取代苯,其中苯环上的一个取代基是氨基;
ii. 分子中含 结构的基团
结构的基团
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
|
⑴汽车内燃机工作时引起反应:N2(g)+O2(g)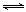 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
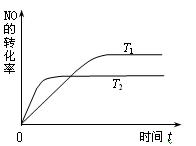
 N2(g)+O2(g)为(填“吸热”或“放热”) ▲ 反应。
N2(g)+O2(g)为(填“吸热”或“放热”) ▲ 反应。
 N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
)设反应①Fe(s)+CO2(g) FeO(s)+CO(g)△H = Q1的平衡常数为K1,
FeO(s)+CO(g)△H = Q1的平衡常数为K1,
反应②Fe(s)+H2O(g) FeO(s)+H2(g)△H = Q2的平衡常数为K 2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g)△H = Q2的平衡常数为K 2,在不同温度下,K1、K2的值如下:
| 温度( T ) |
K1 |
K2 |
| 973 |
1.47 |
2.38 |
| 1173 |
2.15 |
1.67 |
(1)从上表可推断,反应①是_______(填“放”或“吸”)热反应;K2的数学表达式为。
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g)△H = Q3 ①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________。
CO(g)+H2O(g)△H = Q3 ①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________。
| A.缩小容器体积 | B.降低温度 | C.使用合适的催化剂 |
| D.设法减少CO的量E.升高温度 |
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3 =_____________。
有一包白色固体,可能含有NaCl、Na2SO4、CaCl2、CuSO4、Na2CO3 和CaCO3 ,将固体放入水中,经搅拌后为无色溶液,在溶液里加入BaCl2 溶液,产生白色沉淀,再加入盐酸,沉淀全部消失并有气体放出,由此推断:
(1)原固体肯定有______________。
(2)原固体肯定不存在。
(3)__________不能确定存在与否,要确定其存在,应进行的实验是___。
已知X、Y、Z、W四种元素分别是元素周期表中三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z二种元素的元素符号:X_________、Z__________。
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物的结构式为:,它的共价键属于(填:极性、非极性)键;含有离子键和非极性共价键的化合物的电子式为。
(3)由X、Y、Z所形成的常见离子化合物是___________,该化合物与W的最高价氧化物的水化物的浓溶液加热时反应的离子方程式为:_________________________ ;
X与W形成的化合物与水反应时,水作的是(填:氧化剂、还原剂)。