已知碳酸易分解,草酸与碳酸有相似的化学性质,在受热的条件下草酸也会分解,仅生成三种氧化物,我校研究性学习小组对此展开探究:
[提出问题]生成的三种氧化物是什么?
[查阅资料]无水硫酸铜是一种白色粉末物质,遇水变成淡蓝色硫酸铜晶体.化学方程式为:
CuSO4(白色粉末)+5H2O=CuSO4•5H2O(蓝色晶体)
[提出猜想]生成的氧化物中有H2O、CO2和CO。
[实验探究]张亮将生成的气体,依次通过如图所示装置,验证猜想。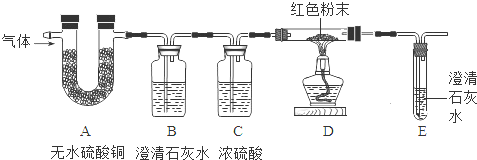
(1)观察到A中 ,证明生成物中有水。
(2)B中澄清石灰水变浑浊,证明 。
(3)D中红色粉末是 (填化学式),实验现象 。
[交流讨论]
陈军认为:张亮不需要E装置也能够推断出生成物中有一氧化碳.你是否支持陈军的观点: (填“支持”或“不支持”),请说出你的理由: 。
陈军还认为:从环保的角度来看,此装置有一个缺陷,请你指出该缺陷: 。
小红同学为探究R、X、Y和Z四种金属的活动性顺序,进行以下实验。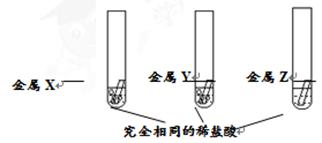
(1)将红色金属R在石棉网上加热,观察到,证明R是铜。
(2)如上图所示,将X、Y和Z分别加入三份完全相同的稀盐酸中,观察到金属X、Y的试管中均有气泡产生,金属Z的试管中无明显现象。
①金属X的试管中,最终还能观察到溶液变为浅绿色,证明X为。
②金属Y可能是(填字母序号)。
| A.Mg | B.Ag | C.Hg | D.Zn |
③四种金属中,在金属活动性顺序表中位于氢后的是,为进一步确定位于氢后金属的活动性相对强弱,还应补充的实验方案为__________(试剂可自选)。
质量守恒定律是化学反应遵循的普遍规律。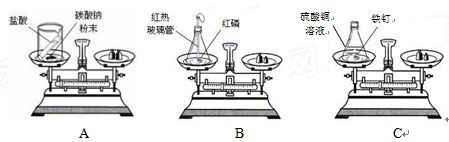
|
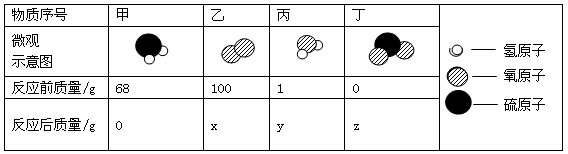
某同学在电视寻宝节目中,看到一些铜制文物上有绿色的锈迹,并对绿色锈迹产生了探究兴趣。
【查阅资料】①绿色锈迹是碱式碳酸铜[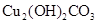 ],受热易分解。
],受热易分解。
②无水硫酸铜为白色粉末,遇水变蓝。
③碱石灰是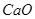 和
和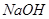 的固体混合物,
的固体混合物,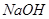 与
与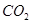 反应生成碳酸钠固体和水。
反应生成碳酸钠固体和水。
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁
上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体的成分。
【猜想与假设】该黑色固体可能是①碳粉;②;③碳和氧化铜的混合物。
【设计方案】请帮助该同学完成下述实验报告。
| 实验操作与现象 |
实验结论 |
| 猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成CO2和H2O。
【进行实验】选择如下图所示装置进行验证。
步骤一:连接A和B,打开活塞,通入一段时间的空气。
步骤二,关闭活塞,依次连接装置A→B→→(填“C”、“D”)。
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
【解释与结论】
①当观察到,说明碱式碳酸铜受热分解生成了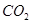 和
和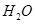 ,写出C中反应的化学方程式。
,写出C中反应的化学方程式。
②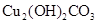 受热分解的化学方程式。
受热分解的化学方程式。
【反思与评价】
上述装置中A的作用是。
兴趣小组设计了测定空气中氧气含量的两套实验装置,请结合图示回答问题(装置气密性良好,注射器的摩擦力忽略不计)。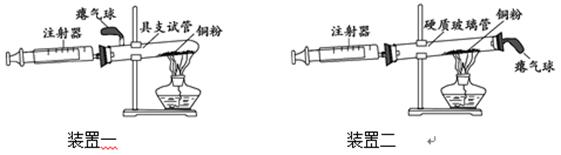
(1)装置一和装置二中气球的位置不同,(填“装置一”或“装置二”)更合理,理由是.
(2)利用合理装置进行实验,记录数据如下。
| 盛有铜粉的仪器中空气体积 |
反应前注射器中空气体积 |
反复推拉注射器,当气球恢复原状时,停止推拉并熄灭酒精灯。观察注射器中气体体积 |
| 25mL |
15mL |
9mL |
分析数据,实验测得空气中氧气的体积分数是。
(3)实验测得的结果出现偏差的原因可能是、.
某校兴趣小组对氢氧化钠溶液与稀盐酸混合后的有关问题,进行了如下探究,请同学们一起参与此次探究之旅。
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
【方案设计】小丽、小林两位同学设计了如下方案进行探究:
| 方案设计者 |
方案步骤 |
方案预估现象 |
方案预估结论 |
| 小丽 |
用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,把试纸呈现的颜色与标准比色卡对照 |
pH=7 |
恰好完全中和 |
| 小林 |
取少量反应后的溶液于一支试管中,并向试管中滴加稀硝酸和硝酸银溶液 |
有白色沉淀生产 |
盐酸过量,没有完全中和 |
【方案评价】请判断以上设计的两个方案中,同学的方案是正确的。
【方案反思】请分析另一个方案错误的原因:。
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】小亮猜想:溶质有NaCl、HCl、NaOH
小丽猜想:溶质只有NaCl
小林猜想:溶质有NaCl、HCl
你的猜想:溶质有(填化学式)
小丽认为小亮的猜想是错误的,她的理由是。
【实验设计及验证】请你将下列实验报告填写完整:
| 实验操作 |
实验现象 |
实验结论 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 |
小林猜想正确 |
|
| 有蓝色沉淀生成 |
你的猜想正确 |