实验室欲用已配好的质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),配制100g质量分数为5%的氢氧化钠溶液,并用此溶液测定某硫酸溶液的溶质质量分数。
(1)配制100g质量分数为5%的氢氧化钠溶液,需要10%的氢氧化钠溶液 g。
(2)配制氢氧化钠溶液时,需要的玻璃仪器有 、滴管、烧杯、玻璃棒。
(3)用配得的氢氧化钠溶液与待测溶质质量分数的硫酸溶液反应,实验过程中溶液的pH变化曲线如图所示:
①根据如图变化曲线,判断进行的操作是 (填字母)。
A.将硫酸溶液逐滴滴加到氢氧化钠溶液中
B.将氢氧化钠溶液逐滴滴加到硫酸溶液中
②b点对应的溶液中的溶质为 (写化学式)。
(4)若完全中和50g稀硫酸溶液,恰好消耗配得的氢氧化钠溶液80g,试计算该稀硫酸的溶质质量分数(请写出计算过程)
(1)下图是实验室常用的制取气体的发生装置和收集装置,根据题目的要求,回答问题。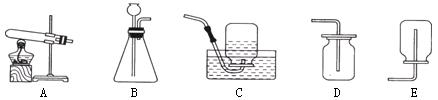
(1)写出装置A中两种玻璃仪器的名称:、。
(2)检查装置A气密性的方法是。
(3)装置A试管口要略向下倾斜的原因是。
(4)若要用高锰酸钾制氧气,发生装置应选择(填序号),试管口要放一团棉花,目的是;该反应的文字表达式是;反应类型是。
(5)收集氧气可以选择装置或(填序号),原因是、。
结合下图所示仪器,回答实验中的有关问题:
(1)用容积为15 mL的试管盛液体加热时,最多可盛液体mL,加热过程中,试管夹应夹持在试管的。
(2)吸取和滴加少量液体的仪器是,用它取用一种试剂后,未经
不可再吸取别的液体,使用过程中应始终保持橡胶胶帽朝 。
(3)向试管内装入碳酸钠粉末时,为避免药品沾在管口和管壁上,可先使试管,
把盛有药品的药匙或纸槽小心地送至试管,然后使试管慢慢直立。
(4)对蜡烛的探究实验:(1)点燃蜡烛,把一根火柴梗放在蜡烛的火焰上(如右图),约1s 后取出,可以看到火柴梗在 处(填字母)最先碳化。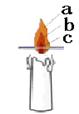
氯化铁溶液能与铜反应生成可溶性的氯化铜和氯化亚铁,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
请回答下列问题:
(1)步骤②③中玻璃棒的作用是。
步骤②实验操作前发生了两个反应:2FeCl3+Fe = 3FeCl2和,
(2)某固体的成分有。
(3)步骤③中产生气体燃烧的化学方程式是。
(4)该流程中可以循环利用的物质是。
下图是某研究性学习小组设计的几种装置,请你分析并回答下列问题: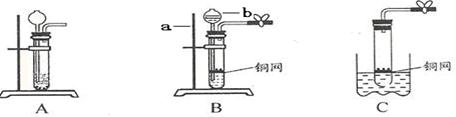
(1)图中标号仪器为:a,b
(2)装置A可用作实验室制取O2或CO2的发生装置,用此装置制取O2的化学方程式是
(3)惠同学从装置A得到启发,在装置A的基础上增加了隔离铜网改成装置B来制取氢气,又用一支底部有一个小洞的试管和矿泉水瓶组合成装置C(夹持仪器都略去)。则B与A相比优点是,C与B相比不同之处是;而装置B显示的化学反应状态为(填“进行中”或“已停止”)。
(4)在实验室用装置C制取CO2的化学反应方程式为,若隔离网改用铁丝做成,则产生的后果是,说明金属活动性FeCu(填“=”或“>”或“<”)
物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙合成丙。甲、乙、丙的微观示意图见下表。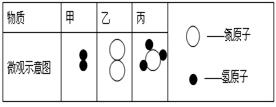
(1)甲、乙、丙三种物质都是由(填“分子”、“原子”或“离子”)构成的。
(2)甲、乙、丙中属于化合物的是(填序号)。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为。
(4)甲和乙合成丙的反应中,甲、乙、丙的微粒个数比为。
(5)现有10 g的甲和60 g的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4 g,则剩余乙的质量为g。