Ⅰ.2009年墨西哥、美国等地出现甲型H1N1流感疫情,引起全世界的关注,这种流感疫情是由甲型H1N1病毒引起的。美国疾病控制和预防中心推荐使用瑞士罗氏制药公司生产的“达菲”胶囊和英国葛兰素—史克公司生产的喷雾式药剂“乐感清”两款药物。
达菲和乐感清的结构简式如下图所示:

请回答下列问题:
(1)乐感清的分子式是____ 。
(2)合成达菲的主要原料莽草酸(结构简式为 
 )存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
)存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
A. 1 mol莽草酸与足量的金属钠反应可生成4mol H2。
B. 1 mol莽草酸与足量氢氧化钠溶液反应,最多可消耗氢氧化钠4 mol。
C. 1 mol莽草酸与足量的碳酸钠溶液反应可生成二氧化碳气体1 mol。
D. 1 mol莽草酸与足量的碳酸氢钠溶液反应可生成二氧化碳气体1 mol
(3)下列每组中各有三对物质,它们都能用分液漏斗分离的是
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,乙二醇和水
Ⅱ.下图中A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物。请回答下列问题:
(1)C分子中官能团的名称是 ;化合物B不能发生的反应是 (填字母序号)。
a.加成反应 b.取代反应 c.消去反应
d.酯化反应 e.水解反应 f.氧化反应
(2)反应②的化学方程式是___________________________。(3) A的结构简式是_________________。
(4)同时符合下列三个条件的B的同分异构体的数目有______个。
a含有间二取代苯环结构 b.属于非芳香酸酯 c.可与FeCl3溶液发生显色反应
写出其中任意一个同分异构体的结构简式__________________________________。
(1)25℃,柠檬水的pH是3,其中c(OH-)==
(2)下列溶液中,c(H+)由小到大的排列顺序是
① 0.1mol/L HCl 溶液 ② 0.1mol/L H2SO4溶液
③ 0.1mol/L NaOH溶液 ④0.1mol/L CH3COOH溶液
(3)在25℃时,1mol· L-1的①(NH4)2SO4 ②CH3COONH4 ③(NH4)2Fe(SO4)2 ④NH4Cl的溶液中,c(NH4+)由大到小的顺序为
(4)pH=3盐酸和pH=11氨水等体积混合后溶液呈性(选填“酸”、“中”或“碱”),溶液中c(NH4+) c(Cl-)(选填“ >”“=”“<” )。
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种。且均符合勒夏 特列原理。请回答下列问题。
特列原理。请回答下列问题。
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应
A(g)+2B(g) 4C(g)
4C(g)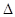 H >0达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是
H >0达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是
①增加C的物质的量②加压③升 温④使用催化剂
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。则图中表示醋酸溶液中pH变化曲线的是(填“A”或“B”)。设盐酸中加入的Zn质量为m1, 醋酸溶液中加入的Zn质量为m2。则m1m2(选填“<”、“=”、“>”)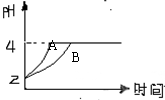
830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g) CO2(g)+H2(g) △H<0试回答下列问题:
CO2(g)+H2(g) △H<0试回答下列问题:
(1)若起始时c(CO)="2" mol·L-1,c(H2O)="3" mol·L -1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
(2)在相同温度下,起始物质按下列四种配比充入该容器中,c(H2O)=2mol·L-1,c(CO)
=c(CO2)="1" mol·L-1, c(H2)="1.5" mol·L-1,则此时该反应是否达到平衡状态(选填“是”与“否”),此时v正v逆(选填“ 大于”、“小于”或“等于”)。
大于”、“小于”或“等于”)。
(3)平衡时若降低温度,该反应的K值将(选填“增 大”、“减小”或“不变”),
大”、“减小”或“不变”),
平衡移动(选填“正向”、“逆向”或“不”)。
(1)在25℃、101kPa下,1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式:。 (2)2Zn(s)+O2(g)=2ZnO(s) Δ
(2)2Zn(s)+O2(g)=2ZnO(s) Δ H1 =" —702" kJ/mol
H1 =" —702" kJ/mol 2Hg(l)+O2(g)=2HgO(s) ΔH2 =" —182" kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2 =" —182" kJ/mol
由此可知ZnO(s)+Hg(l)= Zn(s)+HgO(s) △H3=。
(3)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。右图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:。
(10分)由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图所示的转化关系,已知C是密度最小的气体,甲是电解质。
根据图示转化关系回答:
(1)写出下列物质的化学式:
A________,B________,乙________,丁________。
(2)组成单质A的元素在周期表中的位置是_____________,丙的电子式是
(3)写出下列变化的方程式:
①A与NaOH溶液反应的化学方程式:_______________ ___________________________
___________________________
②乙与过量CO2反应的离子方程式:__________________________________________。