海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示),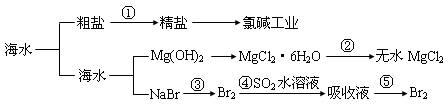
下列有关说法正确的是( )
| A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.加热蒸干氯化镁溶液获得氯化镁固体,通过电解熔融氯化镁冶炼金属镁 |
| C.从第③步到第⑤步的目的是为了富集溴 |
| D.在第③④⑤步中溴元素均被氧化 |
已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理的一项是 
| A.该装置中Cu极为正极 |
| B.当铜极的质量变化为12 .8g时,a极上消耗的O2在标准状况下的体积为2.24L |
| C.b极反应的电极反应式为:H2-2e-=2H+ |
| D.一段时间后锌片质量减少 |
将0.1mol/L的醋酸钠(NaAc)溶液20mL与0.1mol/L盐酸10rnL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是 ( )
| A.c(Ac-)>c(Cl-)>c(H+)>c(HAc) |
| B.c(Ac-)>c(HAc)>c(Cl-)>c(H+)>c(OH-) |
| C.c(Ac-)=c(Cl—)>c(H+)>c(HAc) |
| D.c(Na+)+ c(H+)=c(Ac-)+ c(Cl-)+ c(OH-) |
为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是 ( )
| 选项 |
实验目的 |
主要仪器 |
试剂 |
| A |
分离Br2和CCl4混合物 |
分液漏斗、烧杯 |
Br2和CCl4混合物、蒸馏水 |
| B |
鉴别葡萄糖和蔗糖 |
试管、烧杯、酒精灯 |
葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C |
实验室制取H2 |
试管、带导管的橡皮塞 |
锌粒、稀HNO3 |
| D |
测定NaOH溶液浓度 |
滴定管、锥形瓶、烧杯 |
NaOH溶液、0.1000mol/L盐酸 |
下列除去杂质的方法不正确的是 ( )
| A.除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体 |
| B.除去Na2CO3固体中少量NaHCO3:置于坩埚中加热 |
| C.除去苯中溶有的少量苯酚: 加入适量浓溴水反应后过滤 |
| D.除去FeCl3酸性溶液中少量的FeCl2:通入稍过量的Cl2 |
某无色透明的溶液中,下列各组离子能大量共存的是()
| A.H+、Cl-、Ba2+、CO32- | B.Ag+、I-、K+、NO3- |
| C.K+、OH-、Cl-、Na+ | D.Fe3+、Cl-、NO3-、Na+ |