FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应时生成H2S2,H2S2易分解。实验室用稀硫酸与FeS2颗粒混合,则反应完毕后不可能生成的物质是
| A.H2S | B.S | C.FeS | D.FeSO4 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A.常温常压下,由x g NO2和y g N2O4组成的混合气体中原子总数为3NA,,则x + y ="46" |
| B.1 mol氯气参加氧化还原反应,一定得到NA或2NA个电子 |
| C.1升0.1 mol·L-1 NaBr溶液中,HBr和Br-总和为0.1NA个 |
| D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是 ( )
①碳酸钠溶液与盐酸②硫化氢气体与氯化铁溶液 ③硫酸铝溶液与氨水
④硝酸银溶液与氨水⑤溴化亚铁溶液与氯水 ⑥碳酸氢钙溶液与澄清石灰水
| A.③⑤ | B.①③⑥ | C.②④ | D.②③⑥ |
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
| 物质 编号 |
物质转化关系 |
甲 |
乙 |
丙 |
丁 |
| ① |
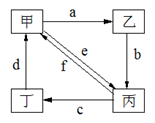 |
Cu |
CuO |
CuSO4 |
Cu(NO3)2 |
| ② |
Na2CO3 |
NaOH |
NaHCO3 |
CO2 |
|
| ③ |
(NH4)2SO3 |
CaSO3 |
SO2 |
NH4HSO3 |
|
| ④ |
Fe |
FeCl3 |
FeCl2 |
Fe(NO)2 |
A.①②③④ B.①②③ C.①③④ D.②④
下列有关物质分类或归类正确的一组是( )
①液氨、液氯、干冰、碘化银均为化合物 ②汽油、盐酸、水玻璃、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质 ④碘酒、牛奶、豆浆、漂粉精均为胶体
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
| A.①和② | B.②和③ | C.③和④ | D.②③⑤ |
下列说法不正确的是( )
| A.欲提高氯水中HClO的浓度可往氯水加适量的碳酸钙粉末 |
| B.形成酸雨的氧化物主要是SO2和氮的氧化物,CO2是造成温室效应的主要气体 |
| C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D.大气中的N2可转化为NO,NO可转化为NO2、硝酸等;含硫物质在自然界中可转化为SO2等含硫化合物 |