X是一种重要的工业原料, X在160℃分解制备异氰酸和氨气,反应方程式为:X  HCNO + NH3(已配平)。完成下列填空:
HCNO + NH3(已配平)。完成下列填空:
(1)在上述反应所涉及的各元素中,原子半径最大的元素是_________,其原子核外电子共占据_______个轨道。
(2)在上述物质中有三种元素处于同周期,下列叙述中能说明三种元素C,N,O非金属性递变规律的事实是____________。
a.最高价氧化物对应水化物的酸性
b.单质与H2反应的难易程度
c.两两形成化合物中元素的化合价
工业上在催化剂条件下,用NH3作为还原剂将烟气中的NOx还原成无害的氮和水,反应方程式可表示为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g)
2N2(g)+3H2O(g)
(3)一定条件下该反应在容积为2L的容器内反应,20 min时达到平衡,生成N2 0.4 mol,则平均反应速率υ(NO)=__________mol/L·min。
(4)当该反应达到平衡时,下列说法一定错误的是___________。
a.气体密度不变 b.气体颜色不变
c.υ(NO)正= 2υ(N2)逆 d.N2和NH3的浓度相等
(5)X可以代替NH3还原烟气中的NOx,X的分子模型如图所示,X电子式为______________。
(6)氰酸有两种结构,一种分子内含有叁键,称为氰酸,另一种分子内不含叁键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。请分别写出氰酸和异氰酸的结构式:_______________、______________。
A-J是中学化学中常见的物质。其中A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。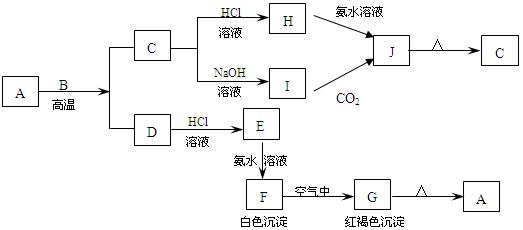
(1)写出下列物质的化学式:
A, J。
(2)按要求书写有关方程式:
D与稀HCl反应的离子方程式;
B与NaOH溶液反应的化学方程式。
(15分)
(1)现有下列物质:维生素A、维生素C、碘元素、铁元素、淀粉、油脂。请选择正确答案填在相应的空格里。
①人体缺乏某种维生素会引起坏血病,这种维生素是____。
②人体缺乏某种微量元素会发生贫血,这种微量元素是______。
③既能为人体提供热量,又能提供必需脂肪酸的物质是_____ ___。
___。
(2)了解一些用药常识,有利于自我保健。现有下列药物:碳酸镁、青霉素、阿司匹林、氢氧化铝。
①其中属于解热镇痛的药物是______。
②青霉素的作用是___。
③碳酸镁可治疗胃酸过多的原理是(用离子方程表示)。
④药片常用淀粉作为黏合剂,淀粉水解的最终产物是________。
(3)生活中处处有化学,化学已渗透到我们的“衣、食、住、行”之中。
①衣:鉴别真假羊毛衫的方法是先取样,再_ ___。
___。
②食:水是人类生存的必需物质。在净水过程中,明矾作为剂;氯气或漂白粉作为剂。
③住:玻璃和钢铁是常用的建筑材料。普通玻璃是由_______等物质组成的;钢铁制品不仅可发生化学腐蚀,在潮湿的空气中还能发生________腐蚀。
④行:铝可用于制造交通工具,铝制品不易生锈的原因是________;橡胶是制造轮胎的重要原料,天然橡胶通过_________措施可增大强度和弹性。
某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+, Ba2+中的几种离子。
Ba2+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是_________。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定有的离子是___________,有关的离子反应式为_____________________________________。
(3)取(2)的滤液加入过量KHSO4溶液,出现白色沉淀,说明原溶液中肯定存在的离子有_______________,有关离子方程____________________________________。
(4)取(3)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有_______________。
(5)原溶液中可能大量存在的阴离子是下列A-D中的(填序号)_________。
| A.Cl- | B.NO3- | C.CO32- | D.OH- |
实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为:
()KMnO4+( )HCl(浓) ===( )KCl+()MnCl2+()Cl2↑+()H2O
(1)请配平化学方程式(将化学计量数填入括号内)。
(2)请将上述配平的化学方程式改写为离子方程式________________。
(3)浓盐酸在反应中显示出来的性质是________________(填写编号,多选倒扣)。
①只有还原性②还原性和酸性
③只有氧化性④氧化性和酸性
(4)产生0.5molCl2,则转移的电子的物质的量为______mol。
(5)已知反应CuS+4HNO3=Cu(NO3)2+2NO2↑+S↓+2H2O,当转移电子数为1.806×1023时,被还原的硝酸的物质的量是,产生标况NO2的体积为。
现有以下物质:① NaCl晶体②液态SO3③液态的醋酸④锌⑤ BaSO4固体⑥纯蔗糖⑦酒精⑧熔化K2SO4,请回答下列问题(用序号填空,多、错、漏均不得分)
(1)以上物质中能导电的是。
(2)以上物质属于电解质的是。
(3)以上物质中属于非电解质的是。