已知25℃时有关弱酸的电离平衡常数:
| 弱酸 |
HCOOH |
HCN |
H2CO3 |
| 电离平衡常数 |
1.77×l0–5 |
4.9×l0–10 |
Ki1=4.3×l0–7 Ki2=5.6×l0–11 |
下列选项错误的是
A.等物质的量浓度的各溶液pH关系为:PH(NaCN)>PH(Na2CO3)>PH(NaHCO3)>PH(HCOONa)
B.2CN– +H2O + CO2 →HCN + CO32–
C.等物质的量浓度的HCN溶液与NaOH溶液等体积混合后溶液中:c(OH–)>c(H+),c(Na+)>c(CN–)
D.NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +2c(CO32–)
某苯的同系物的化学式为C11H16,经测定该分子中除含苯环外,不再含有其它环状结构,分子中还含有2个 —CH3,2个 —CH2— 和1个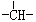 ,则符合该条件的分子结构有:
,则符合该条件的分子结构有:
| A.3种 | B.4种 | C.5种 | D.6种 |
乙烷在光照条件下与氯气混合,最多可能产生物质的种类是:
| A.6种 | B.7种 | C.8种 | D.10种 |
下列分子中的所有碳原子均在同一条直线上的是:
| A.CH3CH2CH2CH3 |
| B.CH3 — CH=CHCH3 |
C.HC≡C—CH2 |
| D.CH3—C≡C—C≡C—CH3 |
下列文字表述与反应方程式对应且正确的是:
| A.甲烷与氯气反应:CH4+4Cl2 → CCl4+4HCl |
| B.用醋酸除去水垢:CaCO3+2H+ ="=" Ca2+ +H2O+CO2↑ |
| C.乙醇和钠反应:2CH3CH2OH+2Na → 2CH3CH2ONa+H2↑ |
D.苯和浓硝酸、浓硫酸的混合物水浴60℃反应: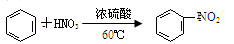 |
下列各组物质中,属于同分异构体且属于碳链异构的是:
| A.CH3CH2CH2CH3和CH3CH(CH3)2 |
| B.CH2=C(CH3)2和CH3CH=CHCH3 |
| C.CH3COOH和HCOOCH3 |
| D.CH3CH2CHO和CH3COCH3 |