硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下: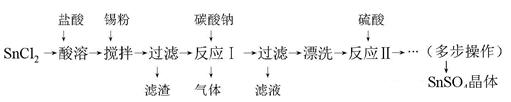
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因 。
(2)加入Sn粉的作用有两个:①调节溶液pH ② 。
(3)反应Ⅰ生成的气体为CO2,得到的沉淀是SnO。该沉淀经过滤后需漂洗,如何证明沉淀已经洗涤完全? 。
(4)多步操作包含的具体实验步骤的名称可以是: 。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 。
(6)该小组通过下列方法测所用锡粉样品的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl→SnCl2 + H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:6FeCl2 + K2Cr2O7 + 14HCl →6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1. 226 g 锡粉样品,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液32.00 mL。则该锡粉样品中锡的质量分数是
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):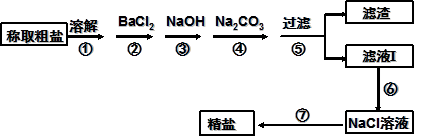
请回答:
(1)步骤⑦需采用的主要物质分离提纯操作,名称是,所需要的实验仪器和用品除铁架台、酒精灯、玻璃棒外,还要。
(2)步骤③加入过量NaOH的目的是:
(3)步骤⑥需加入适量的(填试剂名称),所发生反应的离子方程式为:
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程。其设计的模拟装置如下: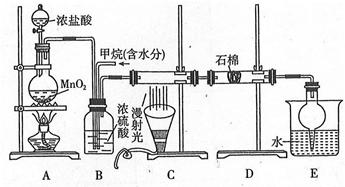
根据要求填空:(1)B装置有三种功能:①均匀混合气体;②③
(2)设V(C12)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应
(3)D装置的石棉中均匀混有K I粉末,其作用是
(4)E装置的作用是(填编号)
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(5)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为(填分离方法名称)
该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为(填编号)。
A.CH4 B.CH3C1 C.CH2C12 D.CHCl3 E.CCl4
已知Fe(OH)2是白色难溶于水的物质,很容易被空气中的氧气氧化为Fe(OH)3。如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化。实验时必须使用铁屑和6mol/L的硫酸,其它试剂自选。
请填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是;
(2)实验开始时应先将活塞E(填“打开”或“关闭”),C中收集到的气体的主要成份是;
(3)简述生成Fe(OH)2的操作过程
(4)(3)操作后拔出装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
请回答该实验中的问题。
(1)写出该反应的反应方程式:;并指明该氧化还原反应的还原剂是,氧化剂是。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是。
(3)实验开始时,应先点燃(填写“酒精灯”或“酒精喷灯”)。
(6分)按图中所示装置,用两种不同操作分别进行实验.回答有关问题:
(1)按图示连接好装置,打开止水夹a,在B中可观察到的现象是,
A中发生反应的化学方程式是;
(2)反应片刻后,夹紧止水夹a,此时可观察到的现象有:____,B中发生反应的离子方程式是:。